题目内容
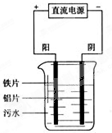 电浮选凝聚法是工业上采用的一种污水处理方法如图是电解污水装置示意图.
电浮选凝聚法是工业上采用的一种污水处理方法如图是电解污水装置示意图.(1)根据污水净化原理写出阳极和阴极的电极反应:
阳极:
阴极:
(2)分析最后底层积聚的一层沉渣是如何沉淀的:
(3)一些悬浮物是怎样形成浮渣的:
考点:电解原理
专题:电化学专题
分析:(1)阳极是活泼金属电极时,该极上是金属电极本身失电子的氧化反应,并且伴随阴离子失电子的氧化反应,阴极上是阳离子得电子的还原反应,据此书写电极反应式;
(2)阳极是活泼金属铁为电极时,该极上是金属铁电极本身失电子,生成亚铁离子,但是亚铁离子不稳定,被氧化为铁离子,碱性环境下变为氢氧化铁,据此回答;
(3)根据阴极上产生的氢气的作用来回答.
(2)阳极是活泼金属铁为电极时,该极上是金属铁电极本身失电子,生成亚铁离子,但是亚铁离子不稳定,被氧化为铁离子,碱性环境下变为氢氧化铁,据此回答;
(3)根据阴极上产生的氢气的作用来回答.
解答:
解:(1)阳极是活泼金属铁电极时,该极上是金属铁电极本身失电子的氧化反应,并且伴随阴离子氢氧根离子失电子的氧化反应,亚铁离子不稳定,被氧化为铁离子,在碱性环境下,铁离子会变为氢氧化铁沉淀下来,阳极反应有:Fe-2e-=Fe2+; 2H2O-4e-=4H++O2↑;4Fe2++10H2O+O2=4Fe(OH)3↓+8H+,阴极上是阳离子得电子的还原反应,即:2H++2e-=H2↑,
故答案为:Fe-2e-=Fe2+; 2H2O-4e-=4H++O2↑;4Fe2++10H2O+O2=4Fe(OH)3↓+8H+;2H++2e-=H2↑;
(2)阳极是活泼金属铁为电极时,该极上是金属铁电极本身失电子,生成亚铁离子,但是亚铁离子不稳定,被氧化为铁离子,碱性环境下变为氢氧化铁,具有吸附作用,能净水,
故答案为:Fe作为阳极,电解时生成Fe2+,Fe2+再被氧化生成Fe3+,Fe3+水解生成Fe(OH)3,Fe(OH)3具有吸附性,可将污染物吸附而沉淀下来;
(3)阴极上是阳离子得电子的还原反应,即:2H++2e-=H2↑,阴极产生H2气泡,气泡把污水中悬浮物带到水面形成浮渣层,
故答案为:阴极产生H2气泡,气泡把污水中悬浮物带到水面形成浮渣层.
故答案为:Fe-2e-=Fe2+; 2H2O-4e-=4H++O2↑;4Fe2++10H2O+O2=4Fe(OH)3↓+8H+;2H++2e-=H2↑;
(2)阳极是活泼金属铁为电极时,该极上是金属铁电极本身失电子,生成亚铁离子,但是亚铁离子不稳定,被氧化为铁离子,碱性环境下变为氢氧化铁,具有吸附作用,能净水,
故答案为:Fe作为阳极,电解时生成Fe2+,Fe2+再被氧化生成Fe3+,Fe3+水解生成Fe(OH)3,Fe(OH)3具有吸附性,可将污染物吸附而沉淀下来;
(3)阴极上是阳离子得电子的还原反应,即:2H++2e-=H2↑,阴极产生H2气泡,气泡把污水中悬浮物带到水面形成浮渣层,
故答案为:阴极产生H2气泡,气泡把污水中悬浮物带到水面形成浮渣层.
点评:本题考查电解原理及其应用,本题注意阳极材料为铁,为活性电极,易被氧化,本题难度不大,注意基础知识的积累.

练习册系列答案
 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案
相关题目
下列说法中正确的是( )
| A、1L水中溶解了58.5gNaCl,该溶液的物质的量浓度为1mol/L |
| B、从1L2mol/L的H2SO4溶液中取出0.5 L,该溶液的浓度为1mol/L |
| C、配制480mL0.5 mol/L的CuSO4溶液,需62.5g胆矾 |
| D、10g98%的硫酸(密度为1.84 g?cm-3)与10 mL18.4 mol?L-1的硫酸的浓度不同 |
下列各组物质,按化合物、单质、混合物顺序排列的是( )
| A、烧碱、液态氧、铁矿石 |
| B、生石灰、白磷、熟石灰 |
| C、干冰、铜、氯化氢 |
| D、空气、氮气、胆矾 |
常温下用石墨电极电解1L 0.01mol?L-1NaCl溶液,电解一段时间后,阴极产生0.04g气体.下列说法正确的是(假设电解过程中溶液体积不变)( )
| A、电解过程中有0.02mol电子转移 |
| B、阳极产物只有氯气 |
| C、在标准状况下,阳极产生的气体体积为0.448L |
| D、电解后溶液的pH=12 |
部分氧化的Fe-Cu合金样品(氧化产物为Fe2O3、CuO) 共5.92g,经如图处理:

下列说法正确的是( )
①滤液A中的阳离子为Fe2+、Fe3+、H+
②样品中含氧元素的物质的量为0.03mol
③溶解样品的过程中消耗硫酸的总物质的量为0.04mol
④V=224mL
⑤V=336mL.

下列说法正确的是( )
①滤液A中的阳离子为Fe2+、Fe3+、H+
②样品中含氧元素的物质的量为0.03mol
③溶解样品的过程中消耗硫酸的总物质的量为0.04mol
④V=224mL
⑤V=336mL.
| A、①③④ | B、②③④ |
| C、②③⑤ | D、①③⑤ |
某温度下,在一个2L的密闭容器中加入4mol A和2mol B进行如下反应:3A(g)+2B(g)?4C(s)+D(g),反应2min后达到平衡,测得生成1.6mol C,下列说法正确的是( )
| A、前2 min D的平均反应速率为0.2 mol?L-1?min-1 |
| B、此时,B的平衡转化率是40% |
| C、增大该体系的压强,平衡不移动 |
| D、增加B,平衡向右移动,B的平衡转化率增大 |
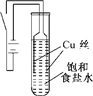 某化学研究小组以铜为电极电解饱和食盐水,探究过程如下:
某化学研究小组以铜为电极电解饱和食盐水,探究过程如下: