题目内容
18.下列叙述中正确的是( )| A. | 液溴易挥发,在存放液溴的试剂瓶中应加水封 | |
| B. | 加入稀盐酸产生无色无味气体,将气体通入澄清石灰水中,溶液变浑浊,则原溶液中一定有CO32- | |
| C. | 向某溶液中加入CCl4,CCl4层显紫色,证明原溶液中存在I- | |
| D. | 加入稀盐酸酸化的AgNO3溶液,产生白色沉淀,则原溶液中一定含有Cl- |
分析 A.溴易挥发,但溴密度大于水;
B.加入稀盐酸产生无色无味气体,将气体通入澄清石灰水中,溶液变浑浊证明生成的气体为二氧化碳,碳酸氢根离子和碳酸根离子都会生成二氧化碳;
C.下层显紫红色,可知碘单质溶解在四氯化碳中;
D.加入稀盐酸酸化,引入Cl-,干扰其检验.
解答 解:A.由于液溴溶于挥发,密度大于水的密度,所以在存放液溴的试剂瓶中应加水封,故A正确;
B.无色无味气体为二氧化碳,则原溶液中存在CO32-或有HCO3-,或二者均存在,故B错误;
C.下层显紫红色,可知碘单质溶解在四氯化碳中,则原溶液存在碘单质,故C错误;
D.加入稀盐酸酸化,引入Cl-,干扰其检验,应加硝酸酸化,故D错误;
故选A.
点评 本题考查物质的检验和鉴别实验方案的设计,为高频考点,把握离子的检验方法、试剂及现象与结论为解答的关键,侧重离子检验的考查,注意检验应排除干扰离子,题目难度不大.

练习册系列答案
相关题目
8.2.0g NaOH固体溶于水配成100mL溶液,溶液中C(Na+)为( )
| A. | 0.2 mol/L | B. | 0.3mol/L | C. | 0.4 mol/L | D. | 0.5 mol/L |
13.下列物质中互为同分异构体的是( )
| A. | 麦芽糖和果糖 | B. | 蔗糖和麦芽糖 | C. | 淀粉和纤维素 | D. | 果糖和葡萄糖 |
3.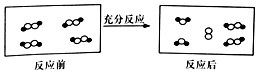 一定条件下,某容器中各微粒在反应前后变化的示意图如图,其中•和○代表不同元素的原子.关于此反应说法正确的是( )
一定条件下,某容器中各微粒在反应前后变化的示意图如图,其中•和○代表不同元素的原子.关于此反应说法正确的是( )
 一定条件下,某容器中各微粒在反应前后变化的示意图如图,其中•和○代表不同元素的原子.关于此反应说法正确的是( )
一定条件下,某容器中各微粒在反应前后变化的示意图如图,其中•和○代表不同元素的原子.关于此反应说法正确的是( )| A. | 属于化合反应 | B. | 属于置换反应 | ||
| C. | 属于氧化还原反应 | D. | 属于复分解反应 |
10.已知反应:NaH+H2O=H2+NaOH,对该反应的判断正确的是( )
| A. | 1mol NaH参加反应失去1mol电子 | B. | 每生成1mol H2转移2mol电子 | ||
| C. | NaH既是氧化剂,又是还原剂 | D. | NaOH是氧化产物 |
7.在碱性溶液中能大量共存且为无色透明的溶液是( )
| A. | K+,Cl-,MnO4-,SO42- | B. | Na+,SiO32-,NO3-,CO32- | ||
| C. | Na+,NO3-,SO42-,HCO3- | D. | Na+,SO42-,S2-,ClO- |
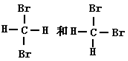
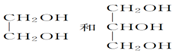

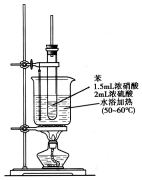 纯硝基苯是一种具有苦杏仁气味的无色油状液体,密度比水大,是制造染料的重要原料,实验室用如图所示的装置来制取.
纯硝基苯是一种具有苦杏仁气味的无色油状液体,密度比水大,是制造染料的重要原料,实验室用如图所示的装置来制取.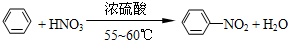 .
.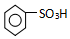 ),导致硝基苯的产率下降.写出发生副反应的化学方程式
),导致硝基苯的产率下降.写出发生副反应的化学方程式 +H2SO4(浓)$\stackrel{△}{→}$
+H2SO4(浓)$\stackrel{△}{→}$