题目内容
10.已知反应:NaH+H2O=H2+NaOH,对该反应的判断正确的是( )| A. | 1mol NaH参加反应失去1mol电子 | B. | 每生成1mol H2转移2mol电子 | ||
| C. | NaH既是氧化剂,又是还原剂 | D. | NaOH是氧化产物 |
分析 NaH中H元素的化合价为-1价,具有强还原性,与水反应时为还原剂,水是氧化剂,每生成1mol氢气转移1mol电子.
解答 解:A.NaH中H元素的化合价为-1价,1mol NaH参加反应失去1mol电子,故A正确;
B.NaH中H元素的化合价为-1价,H2O中H为+1价,生成1mol氢气转移1mol电子,故B错误;
C.与水反应时NaH为还原剂,水为氧化剂,故C错误;
D.该反应中氧化产物和还原产物都是氢气,故D错误;
故选A.
点评 本题考查氧化还原反应,题目难度不大,注意正确判断元素的化合价,根据化合价的变化分析氧化还原反应.

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
20.互为同系物的有机物一定都是( )
| A. | 有相同的分子量 | B. | 有相同的通式 | ||
| C. | 有完全相同的物理性质 | D. | 有完全相同的化学性质 |
1.化学实验有助于理解化学知识,形成化学观念.下列实验操作正确的是( )
| A. | 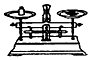 称量药品 | B. | 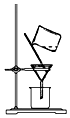 过滤 | C. | 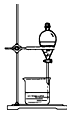 分离乙醇和水 | D. | 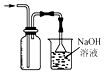 收集HCI |
18.下列叙述中正确的是( )
| A. | 液溴易挥发,在存放液溴的试剂瓶中应加水封 | |
| B. | 加入稀盐酸产生无色无味气体,将气体通入澄清石灰水中,溶液变浑浊,则原溶液中一定有CO32- | |
| C. | 向某溶液中加入CCl4,CCl4层显紫色,证明原溶液中存在I- | |
| D. | 加入稀盐酸酸化的AgNO3溶液,产生白色沉淀,则原溶液中一定含有Cl- |
5.向烧杯中加入25mL蒸馏水,加热至沸腾,向沸水中逐滴加入6滴FeCl3饱和溶液.继续加热至溶液呈红棕色,停止加热,就制得了Fe(OH)3胶体.下列有关胶体的叙述不正确的是( )
| A. | 胶体是一种分散系,属于混合物 | |
| B. | 胶体的本质特征是能发生丁达尔现象 | |
| C. | 胶体粒子直径介于1nm-100nm | |
| D. | 利用丁达尔现象是区分胶体和溶液的一种常用方法 |
2.在恒温恒的密闭容器中,发生反应:A(g)+3B(g)?nC(g).Ⅰ.将1molA和3molB在一定条件下反应,达平衡时C的体积分数为x;Ⅱ.若起始时A、B、C投入的物质的量分别为a、b、c(均不为零),平衡时C的体积分数液为x,下列说法正确的是( )
| A. | 若Ⅰ达平衡时,A、B、C各增加1mol,则C转化率将一定增大 | |
| B. | 若向Ⅰ平衡体系中在加入1molA和3molB,C的体积分数若大于x,可断定n>3 | |
| C. | 若Ⅱ体系起始物质的量满足9a+c=3b,则可判断n=3 | |
| D. | 若n=2,则Ⅱ体系起始物质的量应满足2a+1<b<3 |
6.下列说法正确的是:(NA表示阿伏加德罗常数)( )
| A. | 标准状况下,22.4 L HF中含有的氟原子数目为NA | |
| B. | 0.1 mol/L的NH4HSO4溶液中滴加0.1 mol/L的Ba(OH)2溶液至沉淀刚好完全:c (NH4+)>c (OH-)>c (SO42-)>c (H+) | |
| C. | 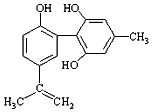 1mol如图物质与浓溴水反应时通常最多消耗Br2为4mol | |
| D. | 常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的△H>0,一定条件下,使用催化剂能加快反应速率并提高反应 物的平衡转化率 |
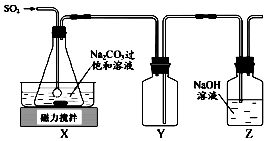 焦亚硫酸钠(Na2S2O5)是常用的抗氧化剂,在空气中,受热时均易分解.实验室制备少量Na2S2O5的方法:在不断搅拌下,控制反应温度在40℃左右,向Na2CO3过饱和溶液中通入SO2,实验装置如图所示.
焦亚硫酸钠(Na2S2O5)是常用的抗氧化剂,在空气中,受热时均易分解.实验室制备少量Na2S2O5的方法:在不断搅拌下,控制反应温度在40℃左右,向Na2CO3过饱和溶液中通入SO2,实验装置如图所示.