题目内容
7.在碱性溶液中能大量共存且为无色透明的溶液是( )| A. | K+,Cl-,MnO4-,SO42- | B. | Na+,SiO32-,NO3-,CO32- | ||
| C. | Na+,NO3-,SO42-,HCO3- | D. | Na+,SO42-,S2-,ClO- |
分析 某强碱性溶液中,含大量的OH-,根据离子之间不能结合生成水、气体、沉淀等,不能发生氧化还原反应等,离子大量共存,并结合离子的颜色来解答.
解答 解:A.该组离子之间不反应,可大量共存,但MnO4-为紫色,与无色不符,故A不选;
B.该组离子碱性条件下不反应,能大量共存,故B选;
C.碱性条件下HCO3-不能大量共存,故C不选;
D.S2-,ClO-发生氧化还原反应而不能大量共存,故D不选.
故选B.
点评 本题考查离子共存,为高频考点,把握习题中的信息及离子之间的反应为解答的关键,侧重复分解反应的离子共存考查,注意归纳常见离子的颜色,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.下列叙述中正确的是( )
| A. | 液溴易挥发,在存放液溴的试剂瓶中应加水封 | |
| B. | 加入稀盐酸产生无色无味气体,将气体通入澄清石灰水中,溶液变浑浊,则原溶液中一定有CO32- | |
| C. | 向某溶液中加入CCl4,CCl4层显紫色,证明原溶液中存在I- | |
| D. | 加入稀盐酸酸化的AgNO3溶液,产生白色沉淀,则原溶液中一定含有Cl- |
2.在恒温恒的密闭容器中,发生反应:A(g)+3B(g)?nC(g).Ⅰ.将1molA和3molB在一定条件下反应,达平衡时C的体积分数为x;Ⅱ.若起始时A、B、C投入的物质的量分别为a、b、c(均不为零),平衡时C的体积分数液为x,下列说法正确的是( )
| A. | 若Ⅰ达平衡时,A、B、C各增加1mol,则C转化率将一定增大 | |
| B. | 若向Ⅰ平衡体系中在加入1molA和3molB,C的体积分数若大于x,可断定n>3 | |
| C. | 若Ⅱ体系起始物质的量满足9a+c=3b,则可判断n=3 | |
| D. | 若n=2,则Ⅱ体系起始物质的量应满足2a+1<b<3 |
6.下列说法正确的是:(NA表示阿伏加德罗常数)( )
| A. | 标准状况下,22.4 L HF中含有的氟原子数目为NA | |
| B. | 0.1 mol/L的NH4HSO4溶液中滴加0.1 mol/L的Ba(OH)2溶液至沉淀刚好完全:c (NH4+)>c (OH-)>c (SO42-)>c (H+) | |
| C. | 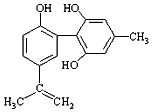 1mol如图物质与浓溴水反应时通常最多消耗Br2为4mol | |
| D. | 常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的△H>0,一定条件下,使用催化剂能加快反应速率并提高反应 物的平衡转化率 |