题目内容
下列化学反应达到平衡后,加压或降温都能使化学平衡向逆反应方向移动的是( )
| A、SO2(g)+NO2(g)?SO3(g)+NO(g) (正反应为放热反应) |
| B、C(s)+CO2(g)?2CO(g) (正反应为吸热反应) |
| C、4NH3(g)+5O2(g)?4NO(g)+6H2O(g) (正反应为放热反应) |
| D、H2S(g)?H2(g)+S(s) (正反应为吸热反应) |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:根据化学平衡移动原理:增大压强,化学平衡向着气体系数和减小的方向进行;升高温度,化学平衡向着吸热方向进行,据此结合选项解答.
解答:
解:A、反应前后体积不变,增大压强平衡不移动,正反应是放热反应,降低温度平衡向正反应移动,故A不选;
B、正反应为体积增大的反应,增大压强,平衡向逆反应移动,正反应是吸热反应,降低温度平衡向逆反应移动,故B选;
C、正反应为体积增大的反应,增大压强,平衡向逆反应移动,正反应是放热反应,降低温度平衡向正反应移动,故C不选;
D、反应前后体积不变,增大压强平衡不移动,正反应是吸热反应,降低温度平衡向逆反应移动,故D不选;
故选B.
B、正反应为体积增大的反应,增大压强,平衡向逆反应移动,正反应是吸热反应,降低温度平衡向逆反应移动,故B选;
C、正反应为体积增大的反应,增大压强,平衡向逆反应移动,正反应是放热反应,降低温度平衡向正反应移动,故C不选;
D、反应前后体积不变,增大压强平衡不移动,正反应是吸热反应,降低温度平衡向逆反应移动,故D不选;
故选B.
点评:本题考查温度和压强对化学平衡移动的影响,注意根据反应特征利用平衡移动原理解答,难度不大.

练习册系列答案
相关题目
在一种能使pH试纸变红色的溶液中,下列离子因发生氧化还原反应而不能大量共存的是( )
①Ag+、Na+、Al3+、Cl-
②Fe2+、NO3-、Cl-、Na+
③K+、Mg2+、CH3COO-、SO42-
④K+、H+、SO32-、I-
⑤Na+、NO3-、SO42-、I-.
①Ag+、Na+、Al3+、Cl-
②Fe2+、NO3-、Cl-、Na+
③K+、Mg2+、CH3COO-、SO42-
④K+、H+、SO32-、I-
⑤Na+、NO3-、SO42-、I-.
| A、②⑤ | B、①②④ |
| C、②③⑤ | D、全部 |
在同温同压下,下列各组热化学方程式中,△H2>△H1的是( )
| A、2H2(g)+O2(g)=2H2O(g);△H1 2H2(g)+O2(g)=2H2O(l);△H2 | ||
| B、S(s)+O2(g)=SO2(g);△H1 S(g)+O2(g)=SO2(g);△H2 | ||
C、CO(g)+
| ||
| D、NaOH(aq)+HCl (aq)=NaCl(aq)+H2O;△H1 NaOH(aq)+CH3COOH (aq)=CH3COONa (aq)+H2O;△H2 |
下列物质属于非电解质,但溶于水后溶液导电的是( )
| A、H2SO4 |
| B、Cl2 |
| C、蔗糖 |
| D、CO2 |
下列说法可以证明反应N2(g)+3H2(g)?2NH3 (g)已达到平衡状态的是( )
| A、1个N2分解的同时,有3个H2的形成 |
| B、1个N2分解的同时,有3个H2的分解 |
| C、1个N2分解的同时,有1个NH3的分解 |
| D、1个N2分解的同时,有2个NH3的形成 |
下列叙述正确的是( )
| A、汽油、柴油和植物油都属于烃 |
| B、乙醇既能被氧化为乙醛也能被氧化为乙酸 |
| C、乙烯和苯加入溴水中,都能观察到褪色现象,原因是都发生了加成反应 |
| D、淀粉和纤维素互为同分异构体 |
在实验室中,下列除去杂志的方法正确的是( )
| A、溴苯中混有溴,有汽油箤取出溴 |
| B、硝基苯中混有浓HNO3和浓H2SO4,将其倒入到NaOH溶液中,静置,分液 |
| C、乙烷中混有乙烯,通氢气在一定条件下反应,使乙烯转化为乙烷 |
| D、乙烯中混有SO2和CO2,将其先后通入NaOH和KMnO4溶液洗气 |
250℃,下列各组离子能大量共存的是( )
| A、pH=1溶液中:K+、Mg2+、AlO2-、S2O32- | ||
| B、Na2S溶液中:SO42-、K+、Cl-、Cu2+ | ||
C、
| ||
| D、含Fe2+溶液中:Na+、ClO-、CH3COO-、HCO3- |
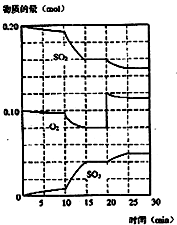 (1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示
(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示