题目内容
250℃,下列各组离子能大量共存的是( )
| A、pH=1溶液中:K+、Mg2+、AlO2-、S2O32- | ||
| B、Na2S溶液中:SO42-、K+、Cl-、Cu2+ | ||
C、
| ||
| D、含Fe2+溶液中:Na+、ClO-、CH3COO-、HCO3- |
考点:离子共存问题
专题:离子反应专题
分析:A.pH=1溶液呈酸性,与H+反应的离子不能大量共存;
B.与S2-反应的离子不能大量共存;
C.
=10-13 mol?L-1 溶液,c(H+)=0.1mol/L,溶液呈酸性;
D.与Fe2+反应的离子不能大量共存.
B.与S2-反应的离子不能大量共存;
C.
| KW |
| c(H+) |
D.与Fe2+反应的离子不能大量共存.
解答:
解:A.pH=1溶液呈酸性,AlO2-、S2O32-与H+反应而不能大量共存,故A错误;
B.Cu2+与S2-反应生成沉淀而不能大量共存,故B错误;
C.
=10-13 mol?L-1 溶液,c(H+)=0.1mol/L,溶液呈酸性,酸性条件下离子之间不发生任何反应,可大量共存,故C正确;
D.ClO-与Fe2+发生氧化还原反应而不能大量共存,故D错误.
故选C.
B.Cu2+与S2-反应生成沉淀而不能大量共存,故B错误;
C.
| KW |
| c(H+) |
D.ClO-与Fe2+发生氧化还原反应而不能大量共存,故D错误.
故选C.
点评:本题考查离子的共存,为高频考点,把握常见离子之间的反应为解答的关键,侧重氧化还原反应、相互促进水解反应及复分解反应的离子共存考查,题目难度不大.

练习册系列答案
相关题目
同质量的下列烃,分别在氧气中充分燃烧,消耗氧气最多的是( )
| A、甲烷 | B、乙炔 | C、丙烯 | D、甲苯 |
下列化学反应达到平衡后,加压或降温都能使化学平衡向逆反应方向移动的是( )
| A、SO2(g)+NO2(g)?SO3(g)+NO(g) (正反应为放热反应) |
| B、C(s)+CO2(g)?2CO(g) (正反应为吸热反应) |
| C、4NH3(g)+5O2(g)?4NO(g)+6H2O(g) (正反应为放热反应) |
| D、H2S(g)?H2(g)+S(s) (正反应为吸热反应) |
在一定温度、恒容条件下,可逆反应:A2(g)+B2(g)?2AB(g)+C(s) 达到化学平衡的标志是( )
| A、单位时间生成nmol的C,同时生成2nmol 的AB |
| B、容器内的总压,不随时间变化 |
| C、容器内气体密度不变 |
| D、单位时间生成n mol的A2,同时生成n mol的B2 |
相同条件下22克下列气体中跟22克二氧化碳的体积相等的是( )
| A、SO2 |
| B、N2 |
| C、N2O |
| D、CO |
在一定温度下,一定体积的容器中,可逆反应:A(g)+3B(g)?2C(g)达到平衡的标志是( )
| A、A、B、C的浓度相等 |
| B、容器中压强不再变化 |
| C、单位时间消耗nmol A,同时生成2n mol C |
| D、A、B、C的分子数比为1:3:2 |
设NA为阿伏加德罗常数,下列说法正确的是( )
| A、利用1mol/L FeCl3溶液制得氢氧化铁胶体的胶粒数目一定小于1NA |
| B、10L 18.4mol?L-1硫酸与64g铜加热反应,生成SO2分子的数目一定小于1NA |
| C、通常状况下,22.4L氯气与烧碱溶液完全反应,转移电子数目一定小于1NA |
| D、标准状况下,22.4LHF所含分子数为1NA |
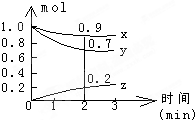 某温度时,在容积为2L的密闭容器中,X、Y、Z三种气体物质的物质的量随时间的变化曲线如图所示,根据图中数据,试回答:
某温度时,在容积为2L的密闭容器中,X、Y、Z三种气体物质的物质的量随时间的变化曲线如图所示,根据图中数据,试回答: