题目内容
15.下列叙述中,正确的是( )| A. | 钢铁腐蚀的负极反应为:Fe-3e-=Fe3+ | |
| B. | Mg-Al及NaOH溶液构成的原电池中负极材料为Mg | |
| C. | 无隔膜电解饱和NaCl溶液所得产物之一是“84”消毒液中的有效成分NaClO | |
| D. | H2-O2燃料电池中电解液为H2SO4,则正极反应式为:O2+4e-=2O2- |
分析 A.钢铁吸氧腐蚀负极铁失电子生成亚铁离子;
B.原电池中失电子的一极为负极;
C.电解饱和NaCl溶液生成氯气、氢气和氢氧化钠;
D.酸性燃料电池中正极上氧气得电子生成水.
解答 解:A.钢铁吸氧腐蚀负极铁失电子生成亚铁离子,则负极反应为:Fe-2e-=Fe2+,故A错误;
B.Al与NaOH溶液反应失电子,Al作负极,Mg作正极,故B错误;
C.电解饱和NaCl溶液生成氯气、氢气和氢氧化钠,氯气与氢氧化钠反应生成次氯酸钠,次氯酸钠是“84”消毒液中的有效成分,故C正确;
D.酸性燃料电池中正极上氧气得电子生成水,则正极反应式为:O2+4H++4e-=2H2O,故D错误.
故选C.
点评 本题考查了原电池原理和电解池原理的应用,注意把握正负极的判断和电极方程式的书写,侧重于考查学生对基础知识的应用能力,题目难度不大.

练习册系列答案
相关题目
6.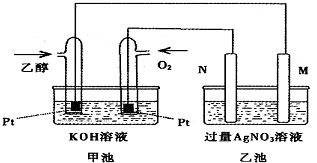 甲乙两池均是电化学装置,按下图连接.乙池中的两个电极分别是石墨电极和铁电极,已知工作过程M、N两个电极的质量均不减少,则下列说法正确的是( )
甲乙两池均是电化学装置,按下图连接.乙池中的两个电极分别是石墨电极和铁电极,已知工作过程M、N两个电极的质量均不减少,则下列说法正确的是( )
 甲乙两池均是电化学装置,按下图连接.乙池中的两个电极分别是石墨电极和铁电极,已知工作过程M、N两个电极的质量均不减少,则下列说法正确的是( )
甲乙两池均是电化学装置,按下图连接.乙池中的两个电极分别是石墨电极和铁电极,已知工作过程M、N两个电极的质量均不减少,则下列说法正确的是( )| A. | M电极的材料是石墨 | |
| B. | 若乙池中某一电极质量增加4.32g时,理论上甲池消耗氧气为224mL | |
| C. | 在此过程中,甲池中OH-向通乙醇的一极移动 | |
| D. | 在此过程中,乙池溶液中电子从M电极向N电极移动 |
5.下列离子方程式书写正确的是( )
| A. | 硫酸溶液与氢氧化钡溶液反应:H++SO42-+OH-+Ba2+═H2O+BaSO4↓ | |
| B. | 氯气溶于水:H2O+Cl2═2H++ClOˉ+Clˉ | |
| C. | 金属钠投入水中:2Na+2H2O═2Na++2OH-+H2↑ | |
| D. | 向氯化铝溶液中加入足量氨水:A13++4NH3•H2O═AlO2-+2H2O+4NH4+ |
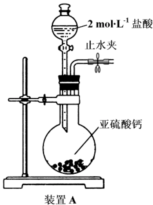


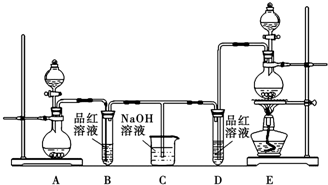
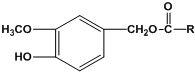 (R为烃基)
(R为烃基)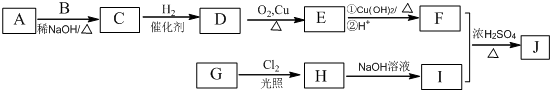
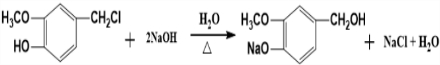 .
. .
.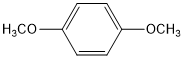 (写结构简式).
(写结构简式).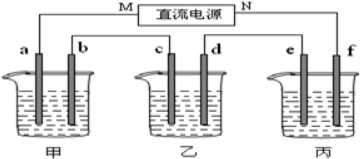
 全球气候变暖已经成为全世界人类面临的重大问题.
全球气候变暖已经成为全世界人类面临的重大问题.