题目内容
2.某学生为探究钠与CO2的反应,利用如下装置进行实验.(已知PdCl2能被CO还原得到黑色的Pd)
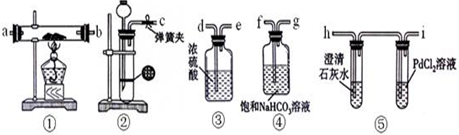
(1)请将如图各装置连接完整(填导气管接口编号,如a、b、c、d等)
c接f,g接d,e接a,b接h,i接、.
(2)装置②制备CO2时具有随开随用,随关随停的功能.简述该装置随关随停的原理关闭弹簧夹后反应生成的气体上部压强增大,到达一定程度后可把反应液压回漏斗,使固液分离从而停止反应;
(3)若用稀盐酸与CaCO3反应制备CO2,在加稀盐酸时,发现CaCO3与稀盐酸不能接触,而稀盐酸又不够了,为使反应能顺利进行,可向长颈漏斗中加入的试剂是ABD.
A.NaNO3溶液 B.CCl4C.苯 D.稀硝酸
(4)检查装置气密性并装好药品后,点燃酒精灯之前应进行的操作是打开弹簧夹,让CO2充满整个装置,当观察到装置⑤中澄清石灰水变浑浊现象时才点燃酒精灯.此步操作的目的是排尽装置中的空气,以免空气中O2、H2O干扰实验
(5)反应过程中CO2足量,假如反应过程中有下列两种情况,分别写出两种情况下钠与CO2反应的化学方程式.
Ⅰ.装置⑤PdCl2溶液中观察到有黑色沉淀,装置①中固体成分只有一种,且向固体中加入稀盐酸产生能使澄清石灰水变浑浊的气体2Na+2CO2$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO
Ⅱ.装置①中钠的质量为0.46g,充分反应后,装置⑤PdCl2溶液中未观察到黑色沉淀,将装置①中的固体加入到足量稀盐酸中产生224mL(标准状况)CO2气体,且溶液中还有固体残留.4Na+3CO2$\frac{\underline{\;\;△\;\;}}{\;}$2Na2CO3+C.
分析 (1)根据实验目的:探究钠与CO2的反应,设计实验方案,完成正确的仪器连接顺序,根据实验目的,②为制取二氧化碳装置,实验室中常用碳酸钙与盐酸反应,二氧化碳中混有氯化氢,需要用装置④除去,然后用装置③干燥,然后在①中进行钠与二氧化碳的反应,然后用⑤检验反应产物,据此进行连接装置;
(2)该装置随关随停的原理式利用弹簧夹控制气体压强,使液体和固体分离停止反应,打开压强减小液体和固体接触继续反应;
(3)所选试剂的作用是增大溶液体积,可以用稀硝酸和硝酸钠溶液,由于四氯化碳的密度大于盐酸,也可以加入四氯化碳溶液,但是苯的密度小于盐酸,加入苯不能使稀盐酸与碳酸钙接触;
(4)二氧化碳与澄清石灰水反应生成碳酸钙沉淀,当装置⑤中澄清石灰水变浑浊说明装置中空气已经排净;原因是空气中的二氧化碳、水与钠反应,需要排净空气,避免干扰实验;(5)Ⅰ.根据题干信息及反应现象判断反应物、生成物,然后写出反应的化学方程式;
Ⅱ.根据n=$\frac{m}{M}$计算出钠的物质的量,再根据n=$\frac{V}{22.4L/mol}$计算出标况下224mL二氧化碳的物质的量,从而得出反应后生成碳酸钠的物质的量;溶液中还有固体残留,该固体只能为C,说明钠与二氧化碳反应生成碳酸钠和C,据此写出反应的化学方程式.
解答 解:(1)根据实验目的,先需要准备二氧化碳,选用二氧化碳发生装置为②,为了便于控制反应,选用的药品是块状碳酸钙,所以只能选用稀盐酸,生成的二氧化碳中混有氯化氢氢气,需要经过装置④饱和碳酸氢钠溶液除去杂质氯化氢,然后干燥二氧化碳,选用装置③浓硫酸,干燥后的二氧化碳通入装置①与金属钠反应,反应后的气体利用装置⑤检验,所以正确的连接顺序为:②④③①⑤,即c接f,g接d,e接a,b接h,i,
故答案为:cfgdeabhi;
(2)随时进行,随时停止的装置,适用于固体和液体不加热反应生成不溶于水的气体制备反应,该装置利用弹簧夹控制气体压强,使液体和固体分离停止反应,打开压强减小液体和固体接触继续反应,
故答案为:关闭弹簧夹后反应生成的气体上部压强增大,到达一定程度后可把反应液压回漏斗,使固液分离从而停止反应;
(3)A.NaNO3溶液:加入硝酸钠溶液后,增大了盐酸的体积,可以使盐酸与碳酸钙接触,故A正确;
B.CCl4:四氯化碳的密度大于稀盐酸,加入四氯化碳后会,四氯化碳层在混合液下层,从而使盐酸与碳酸钙接触,故B正确;
C.苯:苯的密度小于盐酸,加入苯后,苯在混合液上层,无法使稀盐酸与碳酸钙接触,故C错误;
D.稀硝酸:加入稀硝酸后,可以增大溶液体积,使溶液与碳酸钙接触,故D正确;
故答案为:ABD;
(4)钠化学性质比较活泼,能够与空气中的氧气、水反应,所以点燃酒精灯之前应需要打开弹簧夹,让CO2充满整个装置,以便排尽装置中的空气,避免空气中O2、H2O干扰实验,当装置装置⑤中澄清石灰水变浑浊时,证明装置中空气已经排净,
故答案为:打开弹簧夹,让CO2充满整个装置;装置⑤中澄清石灰水变浑浊;排尽装置中的空气,以免空气中O2、H2O干扰实验;
(5)Ⅰ.装置⑤PdCl2溶液中观察到有黑色沉淀,PdCl2能被CO还原得到黑色的Pd,则黑色沉淀为Pd,钠与二氧化碳反应生成了CO;装置①中固体成分只有一种,且向固体中加入稀盐酸产生能使澄清石灰水变浑浊的气体,该气体为二氧化碳,则钠与二氧化碳反应生成碳酸钠和CO,2Na+2CO2$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO,
故答案为:2Na+2CO2$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO;
Ⅱ.装置①中钠的质量为0.46g,钠的物质的量为:n(Na)=$\frac{0.46g}{23g/mol}$=0.02mol,
将装置①中的固体加入到足量稀盐酸中产生224mL(标准状况)CO2气体,二氧化碳的物质的量为:n(CO2)=$\frac{0.224L}{22.4L/mol}$=0.01mol,则反应后生成碳酸钠的物质的量为0.01mol,说明钠完全转化成了碳酸钠;
溶液中还有固体残留,根据化合价变化可知,残留的固体只能为C,则钠与二氧化碳反应生成了碳酸钠和C,反应的化学方程式为:4Na+3CO2$\frac{\underline{\;\;△\;\;}}{\;}$2Na2CO3+C,
故答案为:4Na+3CO2$\frac{\underline{\;\;△\;\;}}{\;}$2Na2CO3+C.
点评 本题考查了探究钠与CO2的反应,涉及了实验装置的连接、化学方程式书写等知识,充分考查了学生的分析、理解能力和灵活应用所学知识的能力,注意依据现象判断反应产物的方法,题目难度中等.

 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案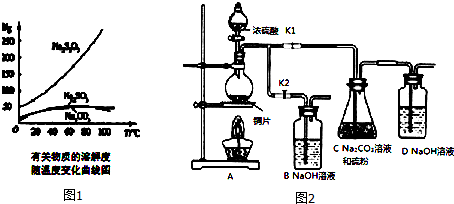
部分操作步骤如下:
①打开K1,关闭K2,向圆底烧瓶中加入足量浓硫酸,加热.
②C中混合液被气流搅动,反应一段时间后,硫粉的量逐渐减少.当C中溶液的pH接近7时,即停止C中的反应,停止加热
③过滤C中的混合液,并将滤液进行处理,得到产品.
(1)步骤①中,圆底烧瓶中发生反应的化学方程式是Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O.
(2)步骤②中,“当C中溶液的pH接近7时即停止C中的反应”的原因是Na2S2O3在酸性溶液中不能稳定存在.“停止C中的反应”的操作是打开K2,关闭K1.
(3)步骤③中,“过滤”用到的玻璃仪器是烧杯、漏斗、玻璃棒(填仪器名称).将滤液进行处理过程是将滤液经过加热浓缩、冷却结晶、过滤、洗涤、烘干,得到产品.依据反应2S2O32-+I2→S4O62-+2I-,可用I2的标准溶液测定产品的纯度.取5.5g产品配制成100mL溶液.取10mL溶液,以淀粉溶液为指示剂,用浓度为0.050mol/L I2的标准溶液进行滴定,相关数据记录如表所示.
| 编号 | 1 | 2 | 3 | 4 |
| 溶液的体积/mL | 10.00 | 10.00 | 10.00 | 10.00 |
| 消耗I2标准溶液的体积/mL | 19.99 | 19.98 | 17.13 | 20.03 |
(5)Na2S2O3•5H2O在产品中的质量分数是90.2%.(计算结果请用百分数表示并保留1位小数)(Na2S2O3•5H2O的式量为248)
| A. | 78g过氧化钠晶体中,含3NA个离子 | |
| B. | 常温常压下,22.4L氦气含有NA个氦原子 | |
| C. | 在O2参与的反应中,1 mol O2作氧化剂时得到的电子数一定是4NA | |
| D. | 常温下16g O2与O3的混合气体中含氧原子数为NA |
| A. | 加NH4Cl溶液 | B. | 加浓氨水 | C. | 加水稀释 | D. | 加NaOH溶液 |
 室温下,若将0.1mol•L-1盐酸滴入20mL 0.1mol•L-1氨水中,溶液pH随加入盐酸体积的变化曲线如图所示.
室温下,若将0.1mol•L-1盐酸滴入20mL 0.1mol•L-1氨水中,溶液pH随加入盐酸体积的变化曲线如图所示. .
.