题目内容
12.亚硫酸钠和硫粉通过化合反应可制得硫代硫酸钠(Na2S2O3).已知:Na2S2O3在酸性溶液中不能稳定存在.有关物质的溶解度随温度变化曲线如图1所示.某研究小组设计了制备Na2S2O3•5H2O的如图2装置图.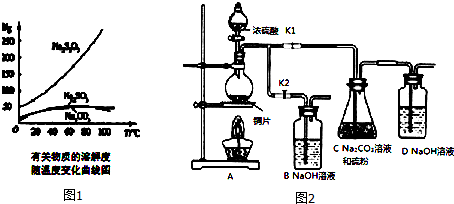
部分操作步骤如下:
①打开K1,关闭K2,向圆底烧瓶中加入足量浓硫酸,加热.
②C中混合液被气流搅动,反应一段时间后,硫粉的量逐渐减少.当C中溶液的pH接近7时,即停止C中的反应,停止加热
③过滤C中的混合液,并将滤液进行处理,得到产品.
(1)步骤①中,圆底烧瓶中发生反应的化学方程式是Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O.
(2)步骤②中,“当C中溶液的pH接近7时即停止C中的反应”的原因是Na2S2O3在酸性溶液中不能稳定存在.“停止C中的反应”的操作是打开K2,关闭K1.
(3)步骤③中,“过滤”用到的玻璃仪器是烧杯、漏斗、玻璃棒(填仪器名称).将滤液进行处理过程是将滤液经过加热浓缩、冷却结晶、过滤、洗涤、烘干,得到产品.依据反应2S2O32-+I2→S4O62-+2I-,可用I2的标准溶液测定产品的纯度.取5.5g产品配制成100mL溶液.取10mL溶液,以淀粉溶液为指示剂,用浓度为0.050mol/L I2的标准溶液进行滴定,相关数据记录如表所示.
| 编号 | 1 | 2 | 3 | 4 |
| 溶液的体积/mL | 10.00 | 10.00 | 10.00 | 10.00 |
| 消耗I2标准溶液的体积/mL | 19.99 | 19.98 | 17.13 | 20.03 |
(5)Na2S2O3•5H2O在产品中的质量分数是90.2%.(计算结果请用百分数表示并保留1位小数)(Na2S2O3•5H2O的式量为248)
分析 (1)铜和浓硫酸加热反应生成硫酸铜、二氧化硫和水;
(2)Na2S2O3在酸性溶液中不能稳定存在,二氧化硫通入碳酸钠溶液中反应生成亚硫酸钠和硫粉反应生成硫代硫酸钠;停止C装置反应打开K2,关闭K1;
(3)依据过滤装置需要的玻璃仪器分析判断;从溶液中获得Na2S2O3•5H2O晶体,需要经过加热浓缩、冷却结晶、过滤、洗涤、烘干等步骤;
(4)以淀粉溶液为指示剂,用浓度为0.050mol/L I2的标准溶液进行滴定,终点现象为溶液变蓝色且半分钟内不褪色;
(5)依据反应的定量关系 2S2O32-+I2→S4O62-+2I-.计算碘单质消耗的硫代硫酸钠,计算得到样品中的质量分数.
解答 解:(1)浓硫酸具有强氧化性,在加热的条件下能氧化单质铜,反应的化学方程式是Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O,
故答案为:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;
(2)生成的SO2和碳酸钠反应生成亚硫酸钠和CO2,由于Na2S2O3在酸性溶液中不能稳定存在,所以C中碳酸钠的作用是起反应物作用及提供碱性环境,“停止C中的反应”的操作是打开K2,关闭K1,
故答案为:Na2S2O3在酸性溶液中不能稳定存在;打开K2,关闭K1;
(3)过滤时的主要玻璃仪器有漏斗、烧杯、玻璃棒,从溶液中获得Na2S2O3•5H2O晶体,需要经过加热浓缩、冷却结晶、过滤、洗涤、烘干等步骤,
故答案为:漏斗、玻璃棒;加热浓缩、冷却结晶;
(4)由于碘遇淀粉显蓝色,则滴定时,达到滴定终点的现象是溶液变蓝,且半分钟不改变,
故答案为:加入最后一滴I2标准溶液后,溶液变蓝,且半分钟内颜色不改变;
(5)根据表中数据可知,第3次实验中消耗I2标准溶液的体积偏小,舍去,则实际消耗I2标准溶液的体积的平均值是$\frac{19.99+19.98+20.03}{3}$mL=20.0mL,则根据反应的方程式可知,Na2S2O3•5H2O的物质的量是0.050mol/L×0.0200L×2×10=0.02mol,所以Na2S2O3•5H2O在产品中的质量分数是$\frac{0.02mol×248g/mol}{5.5g}$=90.2%,
故答案为:90.2%.
点评 本题考查了物质性质的实验验证和实验方法应用,物质性质的掌握和实验基本操作是解题关键,题目难度中等.

 名校课堂系列答案
名校课堂系列答案 用铅蓄电池电解甲、乙电解池中的溶液.已知铅蓄电池的总反应为:Pb+PbO2+2H2SO4═2PbSO4+2H2O,电解一段时间后向c极和d极附近分别滴加酚酞试剂,c极附近溶液变红,下列说法正确的是( )
用铅蓄电池电解甲、乙电解池中的溶液.已知铅蓄电池的总反应为:Pb+PbO2+2H2SO4═2PbSO4+2H2O,电解一段时间后向c极和d极附近分别滴加酚酞试剂,c极附近溶液变红,下列说法正确的是( )| A. | d极为阴极 | |
| B. | 放电时铅蓄电池负极的电极反应式为:PbO2+4H++SO42-+4e-═PbSO4+2H2O | |
| C. | 若利用甲池精炼铜,b极应为粗铜 | |
| D. | 若电极材料均为石墨,当析出6.4g Cu时,两池共产生气体3.36L(标准状况下) |
| 陈述Ⅰ | 陈述Ⅱ | |
| A | BaSO4难溶于水 | SO2气体通入Ba(NO3)2溶液中沉淀 |
| B | 非金属性:Cl>S | 酸性:HClO3>H2SO4 |
| C | 常温下,NaHCO3的溶解度比Na2CO3小 | 向饱和Na2CO3溶液中通入CO2产生沉淀 |
| D | 常温下,SO2与氢硫酸和NaOH溶液均可反应 | SO2是两性氧化物 |
| A. | A | B. | B | C. | C | D. | D |



 .
. 的沸点高.(填高或低)
的沸点高.(填高或低)