题目内容
14.设NA为阿伏加德罗常数值.下列有关叙述正确的是( )| A. | 常温常压下,等质量的N2和CO气体的原子数均为2NA | |
| B. | 在反应KClO4+8HCl=KCl+4Cl2↑+4H2O中,每生成4molCl2转移的电子数为8NA | |
| C. | 含有3mol离子的过氧化钠固体和足量的水反应,电子转移数为NA | |
| D. | 标准状况下,2.24 L CCl4含有的分子数为0.1NA |
分析 A、氮气和CO的摩尔质量相同,且均含2个原子;
B、反应KClO4+8HCl=KCl+4Cl2↑+4H2O生成4mol氯气转移7mol电子;
C、过氧化钠由2个钠离子和1个过氧根构成;
D、标况下四氯化碳为液体.
解答 解:A、氮气和CO的摩尔质量相同,故等质量的两者的物质的量相同,且两者均含2个原子,故等质量的两者中的原子个数相同,但不一定是2NA个,故A错误;
B、反应KClO4+8HCl=KCl+4Cl2↑+4H2O生成4mol氯气转移7mol电子,故当生成4mol氯气时转移7NA个电子,故B错误;
C、过氧化钠由2个钠离子和1个过氧根构成,故含3mol离子的过氧化钠的物质的量为1mol,和水反应转移NA个电子,故C正确;
D、标况下四氯化碳为液体,故不能根据气体摩尔体积来计算其物质的量和分子个数,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.

练习册系列答案
 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
4.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 能使红色石蕊试纸变蓝色的溶液中:K+、CO32-、NO3-、AlO2- | |
| B. | 滴入酚酞溶液显红色的溶液中:K+、Na+、Cu2+、SO42- | |
| C. | 由水电离产生的(H+)=10-13mol/L的溶液中:Na+、Cl-、NO3-、CH3COO- | |
| D. | pH=l 的溶液中:Na+、Fe2+、NO3-、Cl- |
2.下列实验操作中,正确的是( )
| A. |  熄灭酒精灯 | B. |  读取液体体积 | ||
| C. |  移动加热的蒸发皿 | D. |  滴加液体 |
9.关于金属的腐蚀和防护说法不正确的是( )
| A. | 纯的金属在有水的溶液中比不纯的金属(或合金)在其中更容易发生腐蚀 | |
| B. | 金属根据接触的介质的不同,发生腐蚀的化学原理分为:化学腐蚀和电化学腐蚀 | |
| C. | 铝不需要特别的处理就具有抗腐蚀能力 | |
| D. | 在轮船在装上一块锌可以起到保护船身的作用 |
19.下列说法正确的是( )
| A. | 不能发生丁达尔效应的分散系有氯化钠溶液、水等 | |
| B. | 将1 L 2 mol/L的FeCl3溶液制成胶体后,其中含有氢氧化铁胶粒数为2NA | |
| C. | 黄河入海口处三角洲的形成与胶体性质有关 | |
| D. | 电泳现象说明胶体带电 |
6.下列化学反应中,属于氧化还原反应的是( )
| A. | H2SO4+2NaOH═Na2SO4+2H2O | B. | NH3+HCl═NH4Cl | ||
| C. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ | D. | Cl2+2NaOH=NaCl+NaClO+H2O |
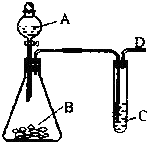 某同学用如图所示的装置来探究SO2的性质及有关实验.
某同学用如图所示的装置来探究SO2的性质及有关实验.