题目内容
15.下列叙述正确的是( )①pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,c(H+)相等
②Na2CO3溶液加水稀释后,恢复至原温度,pH和Kw均减小
③某醋酸溶液的pH=a,将此溶液稀释1倍后,溶液的pH=b,则a>b
④在滴有酚酞溶液的氨水中,加入NH4Cl至溶液恰好无色,则此时溶液的pH<7
⑤1.0×10-3mol/L盐酸的pH=3.0;1.0×10-8mol/L盐酸的pH=8.0
⑥若1mL pH=1的盐酸与100mL NaOH溶液混合后,溶液的pH=7,则NaOH溶液的pH=11.
| A. | ①⑥ | B. | ①② | C. | ③④⑥ | D. | ⑤⑥ |
分析 ①pH=-lgc(H+),pH相等则氢离子浓度相等;
②碳酸钠溶液显碱性,加水稀释碱性减弱,KW只受温度影响,温度不变其不变;
③醋酸溶液加水稀释,溶液酸性减弱;
④酚酞的变色范围为8-10;
⑤常温下,酸溶液的pH<7;
⑥若1mL pH=1的盐酸与100mL NaOH溶液混合后,溶液的pH=7,说明二者的物质的量相等,则NaOH浓度为0.001mol/L.
解答 解:①pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,c(H+)=10-pH,两种溶液的pH相等,所以其c(H+)相等,故正确;
②水的离子积常数只与温度有关,温度不变,则Kw不变,故错误;
③加水稀释醋酸促进电离,但稀释过程中醋酸电离增大程度小于溶液体积增大程度,所以稀释后溶液中c(H+)减小,所以a<b,故错误;
④酚酞的变色范围为8-10,所以在滴有酚酞溶液的氨水中,加入NH4Cl至溶液恰好无色,则此时溶液的pH<8,故错误;
⑤1.0×10-8 mol/L盐酸接近中性,所以该溶液的pH接近7,故错误;
⑥若1mL pH=1的盐酸与100mL NaOH溶液混合后,溶液的pH=7,说明盐酸和NaOH的物质的量相等,则氢氧化钠浓度为盐酸的$\frac{1}{100}$,为0.001mol/L,则NaOH溶液的pH=11,故正确;故选A.
点评 本题考查弱电解质的电离、酸碱混合溶液定性判断、盐类水解等知识点,知道电离平衡常数与盐类水解平衡常数、离子积常数都只与温度有关,与溶液酸碱性及浓度无关,易错选项是⑤,酸或碱溶液接近中性时要考虑水的电离,为易错点.

练习册系列答案
相关题目
6.现有分子式均为C3H6O2的四种有机物A、B、C、D,且分子中均含甲基,把它们分别进行下列实验加以鉴别,实验记录如下:
(1)则A、B、C的结构简式分别为:ACH3CH2COOH,BCH3CH(OH)CHO,CHCOOCH2CH3,
(2)写出D在NaOH溶液中水解的化学方程式CH3COOCH3+NaOH$→_{△}^{水}$CH3COONa+CH3OH.
| NaOH溶液 | 银氨溶液 | 新制Cu(OH)2悬浊液 | 金属钠 | |
| A | 中和反应 | - | 溶解 | 产生氢气 |
| B | - | 有银镜 | 加热后有砖红色沉淀 | 产生氢气 |
| C | 水解反应 | 有银镜 | 加热后有砖红色沉淀 | - |
| D | 水解反应 | - | - | - |
(2)写出D在NaOH溶液中水解的化学方程式CH3COOCH3+NaOH$→_{△}^{水}$CH3COONa+CH3OH.
10.有甲、乙、丙三种物质:
甲: 乙:
乙:
(1)关于乙下列叙述正确的是bd
a.1mol该有机物在加热和催化剂作用下,最多能和2mol NaOH反应
b.该有机物能使酸性KMnO4溶液褪色
c.该有机物的分子式为C9H11Cl
d.该有机物在一定条件下,能发生消去反应、取代反应、氧化反应和还原反应
(2)由甲转化为乙需经下列过程(已略去各步反应的无关产物,下同):
甲$→_{Ⅰ}^{一定条件}$ $→_{Ⅱ}^{一定条件}$Y$→_{Ⅲ}^{一定条件}$乙
$→_{Ⅱ}^{一定条件}$Y$→_{Ⅲ}^{一定条件}$乙
①反应Ⅰ的反应条件是光照
②其中反应II的化学方程式是 +NaOH$→_{△}^{H_{2}O}$
+NaOH$→_{△}^{H_{2}O}$ +NaCl
+NaCl
(3)由甲出发合成丙的路线之一如图:

①写出反应②的化学方程式
②写出C与丙的结构简式 、
、 .
.
甲:
 乙:
乙:
| 丙分子式 | C9H8O |
| 部分性质 | 能使Br2/CCl4褪色 |
a.1mol该有机物在加热和催化剂作用下,最多能和2mol NaOH反应
b.该有机物能使酸性KMnO4溶液褪色
c.该有机物的分子式为C9H11Cl
d.该有机物在一定条件下,能发生消去反应、取代反应、氧化反应和还原反应
(2)由甲转化为乙需经下列过程(已略去各步反应的无关产物,下同):
甲$→_{Ⅰ}^{一定条件}$
 $→_{Ⅱ}^{一定条件}$Y$→_{Ⅲ}^{一定条件}$乙
$→_{Ⅱ}^{一定条件}$Y$→_{Ⅲ}^{一定条件}$乙①反应Ⅰ的反应条件是光照
②其中反应II的化学方程式是
 +NaOH$→_{△}^{H_{2}O}$
+NaOH$→_{△}^{H_{2}O}$ +NaCl
+NaCl(3)由甲出发合成丙的路线之一如图:

①写出反应②的化学方程式

②写出C与丙的结构简式
 、
、 .
.
20.在碱性溶液中能大量共存且溶液为无色透明的离子组是( )
| A. | K+、MnO4-、Na+、Cl- | B. | Fe3+、Na+、Cl-、SO42- | ||
| C. | NH4+、Na+、NO3-、CO32- | D. | Na+、K+、SiO32-、NO3- |
4.在一密闭容器中,反应aA(g)?bB(g)达到平衡后,保持温度不变,将容器体积减小为原来体积的1/2,达到新的平衡时,B的浓度是原来的1.5倍,下列说法正确的是( )
| A. | 平衡向正反应方向移动了 | B. | 物质A的转化率增大 | ||
| C. | 物质B的质量分数减小了 | D. | a>b |
5.将足量锌粉加入Al2(SO4)3、FeSO4、CuSO4、H2SO4混合液中,最后析出的是( )
| A. | Al | B. | Fe | C. | Cu | D. | H2 |
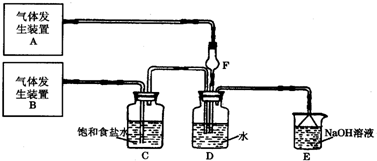
 化学是一门以实验为基础的学科,化学所取得的丰硕成果,是与实验的重要作用分不开的.结合实验装置图回答问题:
化学是一门以实验为基础的学科,化学所取得的丰硕成果,是与实验的重要作用分不开的.结合实验装置图回答问题: