题目内容
3.为了探究Cl2、SO2同时通入H2O中发生的反应,某校化学兴趣小组同学设计了如图所示的实验装置.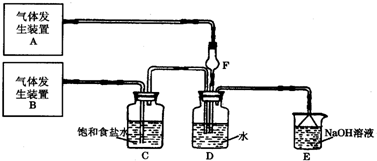
(1)气体发生装置A产生的气体是SO2;
(2)为验证通入D装置中的气体是Cl2过量还是SO2过量,某小组同学准备了以下试剂:
①氯化铁溶液 ②氯化亚铁溶液 ③硫氰化钾溶液
④苯酚溶液 ⑤品红溶液 ⑥酸性高锰酸钾溶液
Ⅰ若Cl2过量:取适量D中溶液滴加至盛有②(选填一个序号,下同)试剂的试管内,再加入③或者④试剂,实验现象是:溶液呈红色或是紫色.
Ⅱ若SO2过量:取适量D中溶液滴加至盛有⑥试剂的试管内,实验现象是:溶液变成无色.
分析 (1)依据实验目的可知A、B气体中,一种是二氧化硫,一种是氯气,制备氯气中含有杂质氯化氢,需要通过饱和食盐水除去氯化氢,据此判断解答;
(2)氯气具有氧化性,能将亚铁离子氧化为铁离子,铁离子遇到硫氰化钾显示红色,遇到酚酞显示紫色;二氧化硫具有还原性,能被高锰酸钾氧化.
解答 解:(1)依据实验目的可知A、B气体中,一种是二氧化硫,一种是氯气,制备氯气中含有杂质氯化氢,需要通过饱和食盐水除去氯化氢,而B气体通入饱和食盐水洗气瓶,所以可知:A为二氧化硫;B为氯气;
故答案为:SO2;
(2)若Cl2过量,因为氯气具有氧化性,能将亚铁离子氧化为铁离子,可以取适量D中溶液滴氯化亚铁,这样亚铁离子氧化为铁离子,加入硫氰化钾或是酚酞,铁离子遇到硫氰化钾显示红色,遇到酚酞显示紫色,局颜色可以判断氯气的存在,
故答案为:②;③或④;溶液呈红色或是紫色;
二氧化硫具有还原性,若SO2过量,加入高锰酸钾,二氧化硫和高锰酸钾之间发生氧化还原反应,使得高锰酸钾褪色,据此确定二氧化硫过量,
故答案为:⑥;溶液变成无色.
点评 本题考查了氯气、二氧化硫的性质,明确物质的性质及发生的化学反应是解答本题的关键,试题培养了学生的分析、理解能力及化学实验能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是( )
| A. | 0.1 mol•L-1 CH3COONa溶液与0.1 mol•L-1 HCl溶液等体积混合:c(Na+)=c(Cl-)>c(CH3COO-)=c(OH-) | |
| B. | 0.1 mol•L-1 NH4Cl溶液与0.1 mol•L-1氨水等体积混合(pH>7):c(NH3•H2O)>c(NH${\;}_{4}^{+}$)>c(Cl-)>c(OH-) | |
| C. | 0.1 mol•L-1 Na2CO3溶液与0.1 mol•L-1 NaHCO3溶液等体积混合:$\frac{2}{3}$c(Na+)=c(CO${\;}_{3}^{2-}$)+c(HCO${\;}_{3}^{-}$)+c(H2CO3) | |
| D. | 0.1 mol•L-1 Na2C2O4溶液与0.1 mol•L-1 HCl溶液等体积混合(H2C2O4为二元弱酸):2c(C2O${\;}_{4}^{2-}$)+c(HC2O${\;}_{4}^{-}$)+c(OH-)=c(Na+)+c(H+) |
18.已知:Na2SO3在空气中会被氧气氧化成Na2SO4.现将物质的量均为1mol的下述物质,长期放置于空气中(最终物质不考虑潮解情况),最后质量增加的大小关系是( )
①Na2O
②Na2O2
③NaOH
④Na2SO3.
①Na2O
②Na2O2
③NaOH
④Na2SO3.
| A. | ①=③>②>④ | B. | ①>②>④>③ | C. | ③>①=②>④ | D. | ④>③>②>① |
8.NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 常温常压下,44 g C3H8中含有的碳碳单键数为3NA | |
| B. | 1mol羟基中电子数为9NA | |
| C. | 室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA | |
| D. | 标准状况下,22.4L 甲醇中含有的氧原子数为1.0NA |
12.科学家发现用二氧化钛(TiO2)作催化剂可以使水在光照条件下分解制得廉价的氢气,这使氢能源的研究和应用更向前迈进了一步.下列说法正确的是( )
| A. | 使用二氧化钛作催化剂使水快速分解的同时放出大量热 | |
| B. | 催化剂的作用是改变反应所需要达到的活化能来增大反应的速率 | |
| C. | 该反应的原理是:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2+O2 | |
| D. | 每产生氢气44.8L,转移电子数目为4NA |
