题目内容
12.如图所示三个烧瓶中分别装人含酚酞的0.01mol/LCH3COONa溶液,并分别放置在盛有水的烧杯中,然后向烧杯①中加入生石灰,向烧杯③中加入NH4NO3晶体,烧杯②中不加任何物质.则下列叙述正确的是( )
| A. | ①说明水解反应为放热反应 | B. | ③说明水解反应为吸热反应 | ||
| C. | ①中溶液红色变浅 | D. | ③中溶液红色变深 |
分析 CaO和水反应是放热反应,所以会导致溶液温度升高,硝酸铵溶解过程吸收热量,会导致溶液温度降低,升高温度促进CH3COONa水解,降低温度抑制CH3COONa水解,据此分析.
解答 解:CaO+H2O=Ca(OH)2,该反应是放热反应,所以会导致溶液温度升高,硝酸铵溶解过程吸收热量,会导致溶液温度降低,升高温度促进CH3COONa水解,溶液的碱性增强,溶液的颜色加深,则①中溶液红色变深;降低温度抑制CH3COONa水解,溶液的碱性减弱,溶液的颜色变浅,③中溶液红色变浅;CH3COONa水解反应为吸热反应,故B正确;
故选:B.
点评 本题考查了盐的水解以及影响水解的因素,题目难度不大,侧重于考查学生的分析能力和对基础知识的应用能力.

练习册系列答案
相关题目
3.已知A、B、C、D的原子序数都不超过18,它们的离子aA(n+1)+、bBn+、cC(n+1)-、dDn-具有相同的电子层结构,则下列说法正确的是( )
| A. | 原子序数:a>b>c>d | |
| B. | 离子半径:A(n+1)+>Bn+>C(n+1)->Dn- | |
| C. | 离子氧化性:A(n+1)+>Bn+离子还原性:C(n+1)->Dn- | |
| D. | C最高价氧化物的水化物的酸性比D的强 |
20.下列各组关于强电解质、弱电解质、非电解质的归类,完全正确的是( )
| 选项 | 强电解质 | 弱电解质 | 非电解质 |
| A | CaCO3 | H2SiO3 | 酒精 |
| B | NaCl | NH3 | BaSO4 |
| C | Fe | CH3COOH | 蔗糖 |
| D | HNO3 | Fe(OH)3 | H2O |
| A. | A | B. | B | C. | C | D. | D |
7.NA为阿伏加德罗常数,下列说的是( )
| A. | 2.24LCO2中含0.3NA原子 | |
| B. | 0.3molNH4NO3固体中含0.3NANH4+ | |
| C. | 5.6g铁粉完全反应一定失去0.3NA电子 | |
| D. | 25℃,0.1NAHCl气体溶于1L水,溶液pH=1 |
17.下列分散系中,明显与其他不同的一种是( )
| A. | 盐酸 | B. | 稀豆浆 | C. | NaOH溶液 | D. | FeCl3溶液 |
4.被誉为“光纤之父”的华裔科学家高锟因为在“光在纤维中的传输用于光学通信”的成就而获 得 2009 年诺贝尔物理学奖,光导纤维的主要成分是( )
| A. | Si | B. | SiO2 | C. | Na2SiO3 | D. | SiCl4 |
3.下列物质中,属于强电解质的是( )
| A. | 醋酸 | B. | Fe(OH)3 | C. | AgNO3 | D. | H2O |
 工业纯碱中常常含有NaCl、Na2SO4等杂质.为测定某工业纯碱的纯度,设计了如右图实验装置.依据实验设计,请回答:
工业纯碱中常常含有NaCl、Na2SO4等杂质.为测定某工业纯碱的纯度,设计了如右图实验装置.依据实验设计,请回答: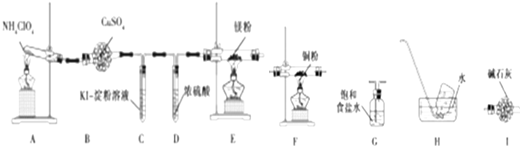
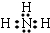 .
.