题目内容
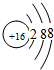
1.用化学用语回答下列问题:(1)画出S2-的结构示意图:
 .
.(2)写出二氧化碳分子的电子式:
 .
.(3)写出氮气分子的结构式N≡N.
分析 (1)S2-的质子数为16,核外电子数为18,各层电子数分别为2、8、8,用小圈和圈内的数字表示原子核和核内质子数,弧线表示电子层,弧线上的数字表示该层的电子数;(2)二氧化碳分子中碳原子与氧原子之间形成2对共用电子对;
(3)用短线“-”代替共用电子对即为结构式,结构式只把共用电子对用短线表示,未成键的电子不画出.
解答 解:(1)S为16号元素,S2-的质子数为16,核外电子数为18,各层电子数分别为2、8、8,硫离子结构示意图为 ,
,
故答案为: ;
;
(2)二氧化碳为直线型结构,分子中存在两个碳氧双键,二氧化碳的电子式为: ,
,
故答案为: ;
;
(3)N原子之间形成三对共用电子对,结构式只把共用电子对用短线表示,未成键的电子不需画出,所以N2的结构式为N≡N,
故答案为:N≡N.
点评 本题考查常用化学用语的书写,题目难度不大,掌握常用化学用语的书写,注意二氧化碳的电子式书写,分子中存在两个碳氧双键,为易错点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.将足量CO2通入下列各溶液中,所含离子还能大量共存的是( )
| A. | H+、NH4+、Al3+、SO42- | B. | K+、SiO32-、Cl-、NO3- | ||
| C. | Na+、S2-、OH-、SO42- | D. | Na+、Fe3+、CH3COO-、HCO3- |
9.设NA为阿伏加德罗常数值.下列有关叙述不正确的是( )
| A. | 标准状况下,2.24 L CCl4含有的共价键数为0.4NA | |
| B. | 0.2 mol C2H6分子中一定存在0.2NA个碳碳单键 | |
| C. | 1 mol Fe溶于过量硝酸,电子转移数为3NA | |
| D. | 14 g乙烯和丙烯混合气体中的氢原子数为2NA |
16.交通警察用经硫酸酸化处理的三氧化铬(CrO3)硅胶检查司机呼出的气体,根据硅胶颜色的变化(硅胶中+6价铬能被酒精蒸气还原为+3价铬,颜色由红色变为绿色),可以判断司机是否酒后驾车.下列有关该反应原理的说法中正确的是( )
| A. | 三氧化铬作还原剂 | B. | 乙醇作还原剂 | ||
| C. | CrO3中Cr被氧化 | D. | 乙醇发生还原反应 |
13.下列说法正确的是( )
| A. | 将足量的Na2O2和Na2O分别加入酚酞试液中,最终溶液均为红色 | |
| B. | Na3N是离子化合物,溶于水后得到的溶液能使无色酚酞试液变红 | |
| C. | 2Na2O2+2H2O═4NaOH+O2↑,是水作还原剂的氧化还原反应 | |
| D. | 过氧化钠会因为与空气中的氧气反应而易变质 |
10.下列金属腐蚀不属于电化学腐蚀的是( )
| A. | 硫酸厂里钢铁设备表面锈迹斑斑 | |
| B. | 夏天,家用铁锅易出现锈斑 | |
| C. | 铝壶里盛装醋酸除水垢,发现漏水 | |
| D. | 自来水铜质龙头与铁管接口处出现红褐色锈斑 |
 与NaOH的醇溶液共热制备CH3-CH=CH2.
与NaOH的醇溶液共热制备CH3-CH=CH2.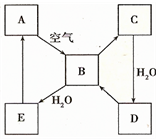 如图表示某淡黄色固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去).B和C的相对分子质量相差16,化合物D是重要的工业原料.
如图表示某淡黄色固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去).B和C的相对分子质量相差16,化合物D是重要的工业原料.