题目内容
17.下列各组物质中,只用一种试剂就能区别的是( )①FeCl2、Al(NO3)3、MgSO4、NH4NO3四种溶液
②MnO2、FeS、CuO、C四种黑色固体
③盐酸、Na2SO4、NaOH三种溶液
④NaCl、AlCl3、Ba(OH)2、HCl四种溶液.
| A. | ①③ | B. | ①②④ | C. | ①②③ | D. | 全部 |
分析 ①阳离子各不相同,可用碱溶液鉴别;
②可用浓盐酸鉴别;
③溶液酸碱性不同;
④可用碳酸氢钠溶液鉴别.
解答 解:①阳离子各不相同,加入氢氧化钠,现象分别为白色絮状沉淀,迅速变为灰绿色,最红变为红褐色;先沉淀后溶解;生成白色沉淀;有刺激性气体生成,可鉴别,故正确;
②加入浓盐酸,加热生成黄绿色气体、生成臭鸡蛋气味的气体、溶液变蓝色,无现象,可鉴别,故正确;
③溶液酸碱性不同,可用pH检验,故正确;
④加入碳酸氢钠溶液,现象分别为无现象、有沉淀和气体生成、生成沉淀、生成气体,可鉴别,故正确.
故选D.
点评 本题考查物质的检验和鉴别,为高频考点,把握物质的性质及性质差异为解答的关键,侧重分析与实验能力的考查,注重实验基础知识的应用,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
7.下列说法中,正确的是( )
| A. | 标准状况下,1mol任何物质的体积都约为22.4L | |
| B. | 1mol任何气体所含分子数都相同,体积也都约为22.4L | |
| C. | 常温常压下,金属Mg从盐酸中置换出1molH2时失去的电子数约1.204×1024 | |
| D. | 同温同压下,相同体积的任何气体单质所含原子数目相同 |
8.NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 在常温常压下,11.2 LN2含有的分子数为0.5 NA | |
| B. | 在常温常压下,1molNe含有的原子数为NA | |
| C. | 71gCl2所含原子数为NA | |
| D. | 在同温、同压下,相同体积的任何气体单质所含的原子数相同 |
5.在一密闭容器中混有CO2、CO、H2三种气体,其平均式量为26.25,投入足量的Na2O2(体积不计)不断用电火花引燃至反应停止,恢复到原温度时,容器内的压强为原来的25%,则混合气体中CO的体积分数为( )
| A. | 20% | B. | 12.5% | C. | 17.5% | D. | 25% |
12.下列关于钠的氧化物的说法正确的是( )
| A. | Na2O2是白色固体,与冷水作用放出氧气,生成氢氧化钠 | |
| B. | 在Na2O2与CO2的反应中,氧化剂是Na2O2,还原剂是CO2 | |
| C. | Na2O不稳定,能继续被氧化,生成Na2O2 | |
| D. | Na2O2能与水反应,生成NaOH,所以Na2O2是碱性氧化物 |
6.在2L容积不变的容器中,发生3A(g)+B(g)?2C(g)+2D(g)的反应.现通入3mol A和2.5mol B,5s内用C表示的反应速率为0.1mol•L-1•s-1,则5s时容器中A的物质的量浓度是( )
| A. | 0.75 mol•L-1 | B. | 1.5 mol•L-1 | C. | 2 mol•L-1 | D. | 0.15 mol•L-1 |
7.下列各说法正确的是( )
| A. | 弱电解质的导电能力一定比强电解质的导电能力弱 | |
| B. | pH=4的醋酸与pH=10的NaOH溶液等体积混合后溶液显碱性 | |
| C. | 豆浆中加入硫酸钙会使蛋白质聚沉. | |
| D. | 同浓度的①NaHCO3②Na2CO3③CH3COONa四种溶液,pH值大小排列顺序是②>①>③ |
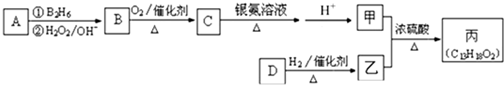
 -CH=CHCHO
-CH=CHCHO -CH2CH2CH2OH
-CH2CH2CH2OH (CH3)2CHCOOCH2CH2CH2-
(CH3)2CHCOOCH2CH2CH2- +H2O
+H2O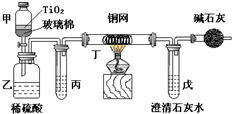 电镀厂曾采用有氰电镀工艺,由于排放的废水中含有的剧毒CN-离子,而逐渐被无氰电镀工艺替代.处理有氰电镀的废水时,可在催化剂TiO2作用下,先用NaClO将CN-离子氧化成CNO-,再在酸性条件下继续被NaClO氧化成N2和CO2.环保工作人员在密闭系统中用下图装置进行实验,以证明处理方法的有效性,并测定CN-被处理的百分率.
电镀厂曾采用有氰电镀工艺,由于排放的废水中含有的剧毒CN-离子,而逐渐被无氰电镀工艺替代.处理有氰电镀的废水时,可在催化剂TiO2作用下,先用NaClO将CN-离子氧化成CNO-,再在酸性条件下继续被NaClO氧化成N2和CO2.环保工作人员在密闭系统中用下图装置进行实验,以证明处理方法的有效性,并测定CN-被处理的百分率.