题目内容
向BaCl2溶液中通入SO2将溶液分置于两支试管中,向一份中加入NaOH溶液,出现白色沉淀A,另一份通入少量Cl2,产生白色沉淀B,试回答下列问题:
(1)若不考虑SO2与水的反应向BaCl2溶液中通入SO2无明显现象,“无明显现象”可能是“不反应”,也可能是“反应但无现象”.此处应为 ,原因是 .
(2)沉淀A的化学式为 ,该沉淀能否溶于稀盐酸? _.
(3)写出生成沉淀B的离子方程式: .
(4)生成2.33 g沉淀B,需消耗标准状况下的Cl2 mL.
(1)若不考虑SO2与水的反应向BaCl2溶液中通入SO2无明显现象,“无明显现象”可能是“不反应”,也可能是“反应但无现象”.此处应为
(2)沉淀A的化学式为
(3)写出生成沉淀B的离子方程式:
(4)生成2.33 g沉淀B,需消耗标准状况下的Cl2
考点:二氧化硫的化学性质,氯气的化学性质
专题:
分析:(1)H2SO3酸性小于盐酸,所以SO2和BaCl2溶液不反应;
(2)SO2和NaOH溶液反应生成Na2SO3,Na2SO3和BaCl2发生复分解反应;亚硫酸盐沉淀能溶于稀盐酸;
(3)氯气具有强氧化性,SO2具有还原性,二者在水溶液里发生氧化还原反应生成H2SO4和盐酸,硫酸和氯化钡发生复分解反应;
(4)B是硫酸钡,根据S原子守恒计算SO2的物质的量,再结合转移电子守恒计算氯气的体积.
(2)SO2和NaOH溶液反应生成Na2SO3,Na2SO3和BaCl2发生复分解反应;亚硫酸盐沉淀能溶于稀盐酸;
(3)氯气具有强氧化性,SO2具有还原性,二者在水溶液里发生氧化还原反应生成H2SO4和盐酸,硫酸和氯化钡发生复分解反应;
(4)B是硫酸钡,根据S原子守恒计算SO2的物质的量,再结合转移电子守恒计算氯气的体积.
解答:
解:(1)H2SO3酸性小于盐酸,亚硫酸和BaCl2混合不符合复分解反应的条件,所以SO2和BaCl2溶液不反应,故答案为:不反应;H2SO3酸性小于盐酸;
(2)SO2和NaOH溶液反应生成亚硫酸钠,亚硫酸钠和BaCl2发生复分解反应生成BaSO3,所以A为BaSO3,BaSO3能溶于稀盐酸,故答案为:BaSO3;
(3)氯气具有强氧化性,二氧化硫具有还原性,二者在水溶液里发生氧化还原反应生成硫酸和盐酸,硫酸和氯化钡发生复分解反应,离子方程式为2H2O+SO2+Cl2+Ba2+=BaSO4↓+2Cl-+4H+,故答案为:2H2O+SO2+Cl2+Ba2+=BaSO4↓+2Cl-+4H+;
(4)B是硫酸钡,n(BaSO4)=
=0.01mol,根据S原子守恒知n(BaSO4)=n(SO2)=0.01mol,
根据转移电子守恒知参加反应的n(SO2)=n(Cl2)=0.01mol,则V(Cl2)=0.01mol×22.4L/mol=0.224L=224mL,
故答案为:224.
(2)SO2和NaOH溶液反应生成亚硫酸钠,亚硫酸钠和BaCl2发生复分解反应生成BaSO3,所以A为BaSO3,BaSO3能溶于稀盐酸,故答案为:BaSO3;
(3)氯气具有强氧化性,二氧化硫具有还原性,二者在水溶液里发生氧化还原反应生成硫酸和盐酸,硫酸和氯化钡发生复分解反应,离子方程式为2H2O+SO2+Cl2+Ba2+=BaSO4↓+2Cl-+4H+,故答案为:2H2O+SO2+Cl2+Ba2+=BaSO4↓+2Cl-+4H+;
(4)B是硫酸钡,n(BaSO4)=
| 2.33g |
| 233g/mol |
根据转移电子守恒知参加反应的n(SO2)=n(Cl2)=0.01mol,则V(Cl2)=0.01mol×22.4L/mol=0.224L=224mL,
故答案为:224.
点评:本题考查二氧化硫、氯气的性质,知道二氧化硫和氯气在水溶液中发生的反应是解本题关键,熟练运用原子守恒、转移电子守恒进行计算,题目难度不大.

练习册系列答案
相关题目
利用反应:2NO(g)+2CO?2CO2(g)+N2(g)△H=-746.8KJ?mol-1可净化汽车尾气,如果要同时提高该反应的速率和NO的转化率,采取的措施是( )
| A、降低温度 |
| B、增大压强 |
| C、升高温度同时充入N2 |
| D、用时将CO2和N2从反应体系中移走 |
若某基态原子的外围电子排布为3d54s1,则下列说法正确的是( )
| A、该元素基态原子中共有7个电子 |
| B、该元素原子核外有3个电子层 |
| C、该元素原子M能层共有5个电子 |
| D、该元素原子最外层可能有1个或2个电子 |
体积相同pH相同的盐酸溶液和醋酸溶液,与氢氧化钠溶液中和时两者消耗氢氧化钠的物质的量( )
| A、相同 | B、中和盐酸的多 |
| C、中和醋酸的多 | D、无法比较 |
 用如图所示装置测定Fe和Fe2O3的混合物中单质铁的质量分数(夹持部分已略去).称取Wg样品置于锥形瓶中,通过分液漏斗加入足量稀硫酸使样品完全溶解.实验前量气管起始读数为a mL,实验后量气管的最终读数为b mL.
用如图所示装置测定Fe和Fe2O3的混合物中单质铁的质量分数(夹持部分已略去).称取Wg样品置于锥形瓶中,通过分液漏斗加入足量稀硫酸使样品完全溶解.实验前量气管起始读数为a mL,实验后量气管的最终读数为b mL.
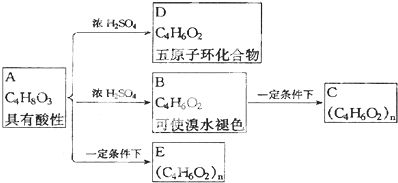
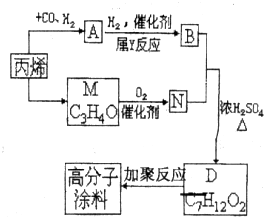 有一种广泛用于汽车、家电产品上的高分子涂料,是按下列流程生产的.图中的(C3H4O)和A都可以发生银镜反应,N和M的分子中碳原子数相等,A的烃基上一氯取代位置有三种.
有一种广泛用于汽车、家电产品上的高分子涂料,是按下列流程生产的.图中的(C3H4O)和A都可以发生银镜反应,N和M的分子中碳原子数相等,A的烃基上一氯取代位置有三种.