题目内容
若某基态原子的外围电子排布为3d54s1,则下列说法正确的是( )
| A、该元素基态原子中共有7个电子 |
| B、该元素原子核外有3个电子层 |
| C、该元素原子M能层共有5个电子 |
| D、该元素原子最外层可能有1个或2个电子 |
考点:原子核外电子排布
专题:原子组成与结构专题
分析:某原子在处于能量最低状态时,外围电子排布为3d54s1,应为Cr元素,位于周期表第ⅥB族,第M层的电子排布为3s23p63d5,以此解答该题.
解答:
解:根据核外电子排布规律,该元素基态原子的电子排布式为1s22s22p63s23p63d54s1.由此可见:该元素原子中共有24个电子,分4个电子层,其中M能层上有13个电子,最外层上有1个电子,如果激发态,最外层可能有2个电子.
A.该元素基态原子中共有24个电子,故A错误;
B.该元素原子核外有4个电子层,故B错误;
C.该元素原子M能层共有13个电子,故C错误;
D.该元素原子最外层上可能有1个或2个电子,故D正确.
故选D.
A.该元素基态原子中共有24个电子,故A错误;
B.该元素原子核外有4个电子层,故B错误;
C.该元素原子M能层共有13个电子,故C错误;
D.该元素原子最外层上可能有1个或2个电子,故D正确.
故选D.
点评:本题考查核外电子排布规律,难度中等,注意构造原理写出元素基态原子的电子排布式.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
已知25℃时有关弱电解质的电离平衡常数:
根据上述电离平衡常数分析,下列推断错误的是( )
| 弱电解质 | 醋酸 | 苯酚 | 碳酸 |
| 电离平衡常数(25℃) | 1.8×10-5 | 1.28×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
| A、25℃时,等物质的量浓度的下列溶液pH关系为:pH(Na2CO3)>pH(C6H5ONa)>pH(NaHCO3)>pH(CH3COONa) |
| B、若amol/L苯酚与bmol/LNaOH两溶液等体积混合后,溶液中c(Na+)=c(C6H5O-),则a一定大于b |
| C、C6H5ONa溶液中通少量CO2气体:2C6H5ONa+H2O=CO2→2C6H5OH+Na2CO3 |
| D、足量的CH3COOH与Na2CO3溶液混合:2CH3COOH+Na2CO3═2CH3COONa+H2O+CO2↑ |
相同温度下,根据三种酸的电离平衡常数,下列判断正确的是( )
| 酸 | HX | HY | HZ |
| K/mol.L-1 | 9×10-7 | 9×10-6 | 2×10-2 |
| A、三种酸的强弱关系:HX>HY>HZ |
| B、反应 HZ+Y-═HY+Z-能够发生 |
| C、相同温度下,0.1mol.L-1的NaX、NaY、NaZ溶液,NaZ溶液pH最大 |
| D、相同温度下,1 mol.L-1HX溶液的电离常数大于0.1 mol?L?1HX |
下列表述中正确的是( )
| A、任何能使熵值增大的过程都能自发进行 |
| B、已知热化学方程式2SO2(g)+O2(g)?2SO3(g)△H=-QkJ?mol-1(Q>0),则将2molSO2(g)和1mol O2(g)置于一密闭容器中充分反应后放出QkJ的热量 |
| C、化学平衡发生移动,平衡常数一定发生变化 |
| D、足量的锌粒分别和等体积同浓度的CH3COOH、HCl反应,两者放出氢气质量相同 |
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中不正确的是( )
| A、氢氧燃料电池在碱性介质中的正极反应式为:O2+2H2O+4e-═4OH- | ||||
B、用铁棒作阳极、碳棒作阴极电解饱和氯化钠溶液的离子方程式为:2C1-+2H2O
| ||||
| C、粗铜精炼时,与电源负极相连的是纯铜,电极反应式为:Cu2++2e-═Cu | ||||
| D、钢铁发生电化学腐蚀的负极反应式为:Fe-2e-═Fe2+ |
下列各组物质,按混合物、单质、化合物顺序排列的是( )
| A、烧碱、液态氧、碘酒 |
| B、空气、氮气、胆矾 |
| C、生石灰、白磷、熟石灰 |
| D、干冰、铁、氯化氢 |
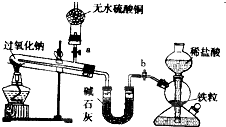 Na2O2是中学化学常用的强氧化剂,除了能与CO2、H2O反应外,还可与其他还原剂如H2、C发生反应,某化学课外兴趣小组为探究Na2O2与H2的反应情况下,设计了如图所示装置进行有关实验.
Na2O2是中学化学常用的强氧化剂,除了能与CO2、H2O反应外,还可与其他还原剂如H2、C发生反应,某化学课外兴趣小组为探究Na2O2与H2的反应情况下,设计了如图所示装置进行有关实验.