题目内容
14. 亚氯酸钠(NaClO2)是重要漂白剂,探究小组开展如下实验,请回答:
亚氯酸钠(NaClO2)是重要漂白剂,探究小组开展如下实验,请回答:[实验Ⅰ]NaClO2晶体按如图装置进行制取.
已知:NaClO2饱和溶液在低于38℃时析出NaClO2•3H2O,高于38℃时析出NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl.
(1)装置C起的是防止D瓶溶液倒吸到B瓶中的作用.
(2)已知装置B中的产物有ClO2气体,则B中产生气体的化学方程式为2NaClO3+Na2SO3+H2SO4=2ClO2↑+2Na2SO4+H2O;装置D中生成NaClO2和一种助燃气体,其反应的化学方程式为2NaOH+2ClO2+H2O2=2NaClO2+2H2O+O2;装置B中反应后的溶液中阴离子除了ClO2-、ClO3-、Cl-、ClO-、OH-外还一定含有的一种阴离子是SO42-;检验该离子的方法是:取少量反应后的溶液于试管中,先加足量的盐酸,再加少量BaCl2溶液,若产生白色沉淀则说明含有SO42-.
(3)从装置D反应后的溶液中获得NaClO2晶体的操作步骤为:①减压在55℃蒸发结晶;②趁热过滤;③用38℃~60℃热水洗涤;④低于60℃℃干燥;得到成品.
(4)反应结束后,打开K1,装置A起的作用是吸收装置B中多余的ClO2和SO2,防止污染空气;如果撤去D中的冷水浴,可能导致产品中混有的杂质是NaClO3和NaCl.
[实验Ⅱ]样品杂质分析与纯度测定
(5)测定样品中NaClO2的纯度:准确称一定质量的样品,加入适量蒸馏水和过量的KI晶体,在酸性条件下发生如下反应:ClO2-+4I-+4H+=2H2O+2I2+Cl-,将所得混合液稀释成100mL待测溶液.取25.00mL待测溶液,加入淀粉溶液做指示剂,用c mol•L-1 Na2S2O3标准液滴定至终点,测得消耗标准溶液体积的平均值为V mL(已知:I2+2S2O32-=2I-+S4O62-),则所称取的样品中NaClO2的物质的量为c•V•10-3mol.
分析 B中反应为NaClO3和Na2SO3在浓H2SO4的作用生成 ClO2和Na2SO4,C可防止倒吸,起到安全瓶的作用,D中加入过氧化氢和氢氧化钠,在低温下反应生成NaClO2,A和E都为尾气处理装置.
(1)装置D中发生气体反应,装置内压强降低,装置C的作用是安全瓶,防止D瓶溶液倒吸到B瓶中;
(2)装置B中制备得到ClO2,所以B中反应为NaClO3和Na2SO3在浓H2SO4的作用生成 ClO2和Na2SO4,装置D反应后的溶液获得NaClO2晶体,装置D中生成NaClO2,Cl元素的化合价降低,双氧水应表现还原性,有氧气生成,结合原子守恒可知,还有水生成,配平书写方程式;B制得的气体中含有SO2,在装置D中被氧化生成硫酸,可以用利用硫酸钡是白色沉淀检验硫酸根;
(3)从溶液中制取晶体,一般采用蒸发结晶、过滤、洗涤、干燥的方法,注意温度控制;
(4)由题目信息可知,应控制温度38℃~60℃,高于60℃时NaClO2分解成NaClO3和NaCl;
(5)根据化学反应可得关系式:NaClO2~2I2~4S2O32-,令样品中NaClO2的物质的量x,根据关系式计算.
解答 解:(1)装置D中发生气体反应,装置内压强降低,装置C的作用是安全瓶,防止D瓶溶液倒吸到B瓶中,故答案为:防止D瓶溶液倒吸到B瓶中;
(2)装置B中制备得到ClO2,反应的化学反应方程式为2NaClO3+Na2SO3+H2SO4=2ClO2↑+2Na2SO4+H2O;装置D反应后的溶液获得NaClO2晶体,装置D中生成NaClO2,Cl元素的化合价降低,双氧水应表现还原性,有氧气生成,结合原子守恒可知,还有水生成,配平后方程式为2NaOH+2ClO2+H2O2=2NaClO2+2H2O+O2;B制得的气体中含有SO2,在装置D中被氧化生成硫酸,溶液中可能存在SO42-;用氯化钡溶液检验SO42-,具体操作:取少量反应后的溶液,先加足量的盐酸,再加BaCl2溶液,若产生白色沉淀,则说明含有SO42-,
故答案为:2NaClO3+Na2SO3+H2SO4=2ClO2↑+2Na2SO4+H2O;2NaOH+2ClO2+H2O2=2NaClO2+2H2O+O2;SO42-;先加足量的盐酸,再加少量BaCl2溶液,若产生白色沉淀则说明含有SO42-;
(3)从溶液中制取晶体,一般采用蒸发结晶、过滤、洗涤、干燥的方法,为防止析出晶体NaClO2•3H2O,应趁热过滤,由题目信息可知,应控制温度38℃~60℃进行洗涤,低于60℃干燥,故答案为:趁热过滤;60℃;
(4)由于ClO2和SO2均有毒,所以反应结束后,打开K1,装置A起的作用是吸收装置B中多余的ClO2和SO2;由题目信息可知,应控制温度38℃~60℃,高于60℃时NaClO2分解成NaClO3和NaCl,所以如果撤去D中的冷水浴,可能导致产品中混有的杂质是NaClO3和NaCl,
故答案为:吸收装置B中多余的ClO2和SO2,防止污染空气;NaClO3和NaCl;
(5)令样品中NaClO2的物质的量n,则:
NaClO2~2I2~4S2O32-
1mol 4mol
n/4 c mol•L-1×V×10-3L
故n=c•V•10-3mol.
故答案为:c•V•10-3 mol.
点评 本题考查亚氯酸钠制备实验的基本操作、亚氯酸钠的性质及中和滴定等知识,为高频考点,理解原理是解题的关键,同时考查学生分析问题、解决问题的能力,难度较大

| A. | KAl(SO4)2═K++Al3++SO42- | B. | NaH2PO4═Na++H2PO4- | ||
| C. | H2S?2H++S2- | D. | NaClO═Na++Cl-+O2- |
| A. | 0.15NA | B. | 0.6NA | C. | 1.2NA | D. | 2.4NA |
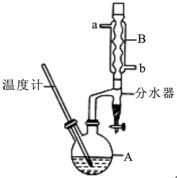 正丁醚常用作有机反应的溶剂.实验室制备正丁醚的反应和主要实验装置如下:2CH3CH2CH2CH2OH$→_{△}^{浓硫酸}$CH3CH2CH2CH2)2O,反应物和产物的相关数据如下表:
正丁醚常用作有机反应的溶剂.实验室制备正丁醚的反应和主要实验装置如下:2CH3CH2CH2CH2OH$→_{△}^{浓硫酸}$CH3CH2CH2CH2)2O,反应物和产物的相关数据如下表:| 相对分子质量 | 沸点/℃ | 密度/(g/cm3) | 水中的溶解性 | |
| 正丁醇 | 74 | 117.2 | 0.8109 | 微溶 |
| 正丁醚 | 130 | 142.0 | 0.7704 | 几乎不溶 |
②加热A中反应液,迅速升温至135℃,维持反应一段时间.
③分离提纯:待A中液体冷却后将其缓慢倒入盛有70mL水的温度分液漏斗中,振摇后静置,分液得粗产物.
④粗产物依次用40mL水、20mL NaOH溶液和40mL水洗涤,分液后加入约3g无水氯化钙颗粒,静置一段时间后弃去氯化钙.
⑤将上述处理过的粗产物进行蒸馏,收集馏分,得纯净正丁醚11g.请回答:
(1)步骤①中浓硫酸和正丁醇的添加顺序为:应先加正丁醇.
(2)加热A前,需先从b(填“a”或“b”)口向B中通入水.
(3)步骤③的目的是初步洗去浓H2SO4,振摇后静置,粗产物应上(填“上”或“下”)口倒出.
(4)步骤④中最后一次水洗的目的为洗去有机层中残留的NaOH及中和反应生成的盐Na2SO4.
(5)步骤⑤中,加热蒸馏时应收集D(填选项字母)左右的馏分.
A.100℃B.117℃C.135℃D.142℃
(6)反应过程中会观察到分水器中收集到液体物质,且分为上下两层,随着反应的进行,分水器中液体逐渐增多至充满时,上层液体会从左侧支管自动流回A.分水器中上层液体的主要成分为正丁醇,下层液体的主要成分为水.
(7)本实验中,正丁醚的产率为34%(精确到1%).
| A. | 浓H2SO4有强氧化性,常温下能与Cu发生剧烈反应 | |
| B. | 金刚石是自然界中硬度最大的物质,不可能与氧气发生反应 | |
| C. | 明矾[KAl(SO4)2•12H2O]在水中能形成Al(OH)3胶体,可用作净水剂 | |
| D. | 将SO2通入品红溶液中,溶液褪色后加热恢复原色;将SO2通入溴水,溴水褪色后加热也能恢复原色 |
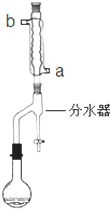 在苹果、香蕉等水果的果香中存在着乙酸正丁酯.某化学课外兴趣小组欲以乙酸和正丁醇为原料合成乙酸正丁酯.实验步骤如下:
在苹果、香蕉等水果的果香中存在着乙酸正丁酯.某化学课外兴趣小组欲以乙酸和正丁醇为原料合成乙酸正丁酯.实验步骤如下: