题目内容
请写出下列化学反应的化学方程式:
(1)乙烯的实验室制法: 由甲苯在一定条件下制取TNT: 由丙烯腈CH2=CH-CN制腈纶(聚丙烯腈):
(2)氯化铵水溶液呈酸性: 用氧化铁炼铁(利用铝热法): .
(1)乙烯的实验室制法:
(2)氯化铵水溶液呈酸性:
考点:有机物的结构和性质,盐类水解的应用,金属冶炼的一般原理
专题:
分析:(1)实验室用乙醇和浓硫酸加热到170℃反应制备乙烯;用甲苯和浓硝酸在浓硫酸作用下制备TNT;CH2=CH-CN发生加聚反应制备聚丙烯腈;
(2)氯化铵为强酸弱碱盐,水解成酸性;高温条件下,铝和氧化铁发生置换反应生成铁.
(2)氯化铵为强酸弱碱盐,水解成酸性;高温条件下,铝和氧化铁发生置换反应生成铁.
解答:
解:(1)实验室用乙醇和浓硫酸加热到170℃反应制备乙烯,方程式为CH3CH2OH
CH2=CH2↑+H2O,
用甲苯和浓硝酸在浓硫酸作用下制备TNT,方程式为 ;
;
CH2=CH-CN发生加聚反应制备聚丙烯腈,方程式为nCH2═CHCN
 ,
,
故答案为:CH3CH2OH
CH2=CH2↑+H2O; ;
;
nCH2═CHCN
 ;
;
(2)氯化铵为强酸弱碱盐,水解成酸性,水解方程式为NH4Cl+H2O NH3.H2O+HCl;
NH3.H2O+HCl;
高温条件下,铝和氧化铁发生置换反应生成铁,方程式为Fe2O3+2Al
2Fe+Al2O3,
故答案为:NH4Cl+H2O NH3.H2O+HCl;Fe2O3+2Al
NH3.H2O+HCl;Fe2O3+2Al
2Fe+Al2O3.
| 浓H2SO4 |
| 170℃ |
用甲苯和浓硝酸在浓硫酸作用下制备TNT,方程式为
 ;
;CH2=CH-CN发生加聚反应制备聚丙烯腈,方程式为nCH2═CHCN
| 催化剂 |
 ,
,故答案为:CH3CH2OH
| 浓H2SO4 |
| 170℃ |
 ;
;nCH2═CHCN
| 催化剂 |
 ;
;(2)氯化铵为强酸弱碱盐,水解成酸性,水解方程式为NH4Cl+H2O
 NH3.H2O+HCl;
NH3.H2O+HCl;高温条件下,铝和氧化铁发生置换反应生成铁,方程式为Fe2O3+2Al
| ||
故答案为:NH4Cl+H2O
 NH3.H2O+HCl;Fe2O3+2Al
NH3.H2O+HCl;Fe2O3+2Al
| ||
点评:本题考查较为综合,涉及有机物结构和性质,盐类的水解以及铝热反应等知识,为高频考点,侧重于学生的分析能力和基础知识的综合理解和运用的考查,难度不大,注意相关基础知识的积累.

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目
下列离子在水溶液中能大量共存的是( )
| A、Ca2+、K+、Cl-、CO32- |
| B、Ba2+、Cl-、K+、SO42- |
| C、Fe3+、Cl-、K+、NO3- |
| D、Ag+、NO3-、K+、Cl- |
下列说法中正确的是( )
| A、含有碳碳双键的有机物均有顺反异构 |
| B、乙烯和聚乙烯均能使酸性KMnO4溶液褪色 |
| C、利用电石与水反应制取C2H2时,可采用CuSO4溶液除去杂质气体 |
| D、苯酚与甲醇在酸性条件下聚合生成酚醛树脂 |
现有四组混合物:①含有水分的植物油;②碘的CCl4溶液;③混有沙子的食盐水溶液;④氯化钠和单质碘的水溶液.分离以上各混合液的正确方法依次是( )
| A、分液、蒸馏、过滤、萃取 |
| B、萃取、蒸馏、分液、蒸馏 |
| C、分液、萃取、过滤、萃取 |
| D、蒸馏、萃取、过滤、分液 |
有按如下特点排列的一系列(n种)稠环芳香烃:
①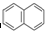 ②
② ③
③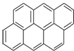 ④
④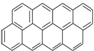 …该系列化合物中所含碳的质量分数最大值是( )
…该系列化合物中所含碳的质量分数最大值是( )
①
 ②
② ③
③ ④
④ …该系列化合物中所含碳的质量分数最大值是( )
…该系列化合物中所含碳的质量分数最大值是( )| A、93.8% | B、95.7% |
| C、97.3% | D、无法确定 |
 (1)维生素C的结构简式是
(1)维生素C的结构简式是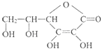 ,维生素C的分子式是
,维生素C的分子式是