题目内容
下列各项表达中正确的是( )
A、O2-的结构示意图为: |
| B、Mg2+的电子式:Mg2+ |
C、NaCl的电子式为:Na  |
| D、N2的结构式为::N≡N: |
考点:电子式、化学式或化学符号及名称的综合
专题:化学用语专题
分析:A.氧离子核电荷数错误,应该为8,表示10;
B.镁离子为简单阳离子,直接用离子符号表示其电子式;
C.氯化钠为离子化合物,阴阳离子需要标出所带电荷;
D.氮气的结构式中不需要标出氮原子的1对孤对电子.
B.镁离子为简单阳离子,直接用离子符号表示其电子式;
C.氯化钠为离子化合物,阴阳离子需要标出所带电荷;
D.氮气的结构式中不需要标出氮原子的1对孤对电子.
解答:
解:A.氧离子的核电荷数为8,核外电子总数为10,正确的离子结构示意图为: ,故A错误;
,故A错误;
B.镁离子为简单的阳离子,其电子式直接用离子符号表示,所以Mg2+的电子式为:Mg2+,故B正确;
C.氯化钠为离子化合物,电子式中需要标出阴阳离子所带的电荷,氯化钠正确的电子式为: ,故C错误;
,故C错误;
D.氮气的电子式为 ,用短线替代共用电子对即为结构式,氮气的结构式为:N≡N,故D错误;
,用短线替代共用电子对即为结构式,氮气的结构式为:N≡N,故D错误;
故选B.
 ,故A错误;
,故A错误;B.镁离子为简单的阳离子,其电子式直接用离子符号表示,所以Mg2+的电子式为:Mg2+,故B正确;
C.氯化钠为离子化合物,电子式中需要标出阴阳离子所带的电荷,氯化钠正确的电子式为:
 ,故C错误;
,故C错误;D.氮气的电子式为
 ,用短线替代共用电子对即为结构式,氮气的结构式为:N≡N,故D错误;
,用短线替代共用电子对即为结构式,氮气的结构式为:N≡N,故D错误;故选B.
点评:本题考查了电子式、结构式、粒子结构示意图的表示方法判断,题目难度中等,注意掌握常见的化学用语的概念及正确的表示方法,明确离子化合物与共价化合物的判断方法及其电子式的区别.

练习册系列答案
 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案
相关题目
下列所得溶液的物质的量浓度等于0.1mo/L的是( )
| A、将0.1mol氨气充分溶解在1L水中 |
| B、将10g质量分数为98%的硫酸与990g水混合 |
| C、将8g三氧化硫溶于水并配成1L溶液 |
| D、将0.1mol氧化钾溶于水并配成1L溶液 |
设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A、标准状况下,22.4 L水的分子数为NA |
| B、常温下将23gNa投入到0.5 L 1.0mol?L-1的盐酸中反应共转移的电子数为0.5NA |
| C、0.5 mol?L-1KCl溶液中含有0.5NA个K+ |
| D、0.7mol的Na2O 和 Na2O2 固体中加入等量且足量的水,所得NaOH溶液浓度相同 |
已知R2+离子核外有a个电子,b个中子,表示R原子符号正确的是( )
A、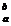 R R |
B、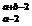 R R |
C、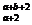 R R |
D、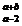 R R |
下列叙述正确的是( )
| A、摩尔是七个基本物理量之一 |
| B、1 mol任何物质都含有6.02×1023个分子 |
| C、标准状况下,1 mol任何物质体积均为22.4 L |
| D、摩尔质量在数值上等于该物质的相对分子质量或相对原子质量 |
下列离子方程式书写正确的是( )
| A、碳酸氢钙溶液中加入少量的氢氧化钠溶液:Ca2++HCO3-+OH-=CaCO3↓+H2O |
| B、硫酸铜溶液与氢氧化钡溶液反应:SO42-+Ba2+═BaSO4↓ |
| C、钠跟水反应:Na+2H2O=Na++2OH-+H2↑ |
| D、NaOH溶液中通入过量SO2:2OH-+SO2═SO32-+H2O |
