题目内容
下列离子方程式书写正确的是( )
| A、碳酸氢钙溶液中加入少量的氢氧化钠溶液:Ca2++HCO3-+OH-=CaCO3↓+H2O |
| B、硫酸铜溶液与氢氧化钡溶液反应:SO42-+Ba2+═BaSO4↓ |
| C、钠跟水反应:Na+2H2O=Na++2OH-+H2↑ |
| D、NaOH溶液中通入过量SO2:2OH-+SO2═SO32-+H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.氢氧化钠少量,离子方程式按照氢氧化钠的组成书写;
B.离子方程式中漏掉了铜离子与氢氧根离子生成氢氧化铜沉淀的反应;
C.根据电荷守恒判断,该离子方程式两边电荷不相等;
D.二氧化硫过量,反应生成亚硫酸氢钠.
B.离子方程式中漏掉了铜离子与氢氧根离子生成氢氧化铜沉淀的反应;
C.根据电荷守恒判断,该离子方程式两边电荷不相等;
D.二氧化硫过量,反应生成亚硫酸氢钠.
解答:
解:A.碳酸氢钙溶液中加入少量的氢氧化钠溶液,碳酸氢根离子部分参与反应,反应的离子方程式为:Ca2++HCO3-+OH-=CaCO3↓+H2O,故A正确;
B.硫酸铜溶液与氢氧化钡溶液反应生成氢氧化铜沉淀和硫酸钡沉淀,正确的离子方程式为:SO42-+Ba2++Cu2++2OH-=Cu(OH)2↓+BaSO4↓,故B错误;
C.钠跟水反应生成氢氧化钠和氢气,正确的离子方程式为:2Na+2H2O=2Na++2OH-+H2↑,故C错误;
D.二氧化硫过量,反应生成亚硫酸氢根离子,正确的离子方程式为:OH-+SO2═HSO3-,故D错误;
故选A.
B.硫酸铜溶液与氢氧化钡溶液反应生成氢氧化铜沉淀和硫酸钡沉淀,正确的离子方程式为:SO42-+Ba2++Cu2++2OH-=Cu(OH)2↓+BaSO4↓,故B错误;
C.钠跟水反应生成氢氧化钠和氢气,正确的离子方程式为:2Na+2H2O=2Na++2OH-+H2↑,故C错误;
D.二氧化硫过量,反应生成亚硫酸氢根离子,正确的离子方程式为:OH-+SO2═HSO3-,故D错误;
故选A.
点评:本题考查了离子方程式的正误判断,该题是高考中的高频题,属于中等难度的试题,注意明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等.

练习册系列答案
相关题目
用NA表示阿伏加德罗常数的值,下列判断错误的是( )
| A、NA个H+的质量为1g |
| B、2L0.5mol/LNa2SO4溶液中含NA个Na+ |
| C、32gO2中含有2NA个O原子 |
| D、标准状况下,1molH2O中含有NA个分子 |
下列化学用语或模型正确的是( )
A、氯化氢的电子式: |
| B、8个中子的碳原子:12C |
C、硫离子结构示意图: |
D、CH4分子的比例模型: |
下列各项表达中正确的是( )
A、O2-的结构示意图为: |
| B、Mg2+的电子式:Mg2+ |
C、NaCl的电子式为:Na  |
| D、N2的结构式为::N≡N: |
用NA表示阿伏加德罗常数,下列叙述中,正确的是( )
| A、常温常压下,11.2 L氯气所含的原子数为NA |
| B、常温常压下,1 molCl2与石灰乳完全反应转移电子数为NA |
| C、NA个氧分子和NA个氦分子的质量比等于4:1 |
| D、1.9 g的H3O+离子中含有的质子数为1.0 NA |
下列物质属于纯净物的是( )
| A、冰水混合物 | B、洁净的空气 |
| C、食醋 | D、清澈的海水 |
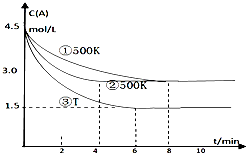 某反应2A(g)?2B(g)+C(g)(吸热反应)在三种不同条件下进行,B、C的起始浓度为0,A的浓度(mol/L)随反应时间(min)的变化情况如图所示.
某反应2A(g)?2B(g)+C(g)(吸热反应)在三种不同条件下进行,B、C的起始浓度为0,A的浓度(mol/L)随反应时间(min)的变化情况如图所示.