题目内容
现有可逆反应:A(g)+B(g)?xC(g),在不同条件下生成物C在反应混合物中的体积分数(C%)与反应时间(t)的关系如图所示,请根据图象回答下列问题:

(1)若甲图中分别表示有催化剂和无催化剂的情况,则 曲线表示无催化剂的情况(填字母,下同);
(2)根据乙图可判断该可逆反应的正反应为 热反应(填“放”或“吸”);
(3)化学计量数x的值 (填取值范围);
(4)若丙图表示反应达到平衡后再充入惰性气体的情况,则 曲线表示恒温恒容的情况.

(1)若甲图中分别表示有催化剂和无催化剂的情况,则
(2)根据乙图可判断该可逆反应的正反应为
(3)化学计量数x的值
(4)若丙图表示反应达到平衡后再充入惰性气体的情况,则
考点:物质的量或浓度随时间的变化曲线
专题:化学平衡专题
分析:(1)使用催化剂,加快反应速率,缩短到达平衡的时间;
(2)由乙图可知,相同压强温度越高,C%越大,说明升高温度,平衡向正反应移动;
(3)温度相同压强越高,C%越小,说明增大压强,平衡向逆反应移动;
(4)恒温恒容条件下,通入惰性气体,不影响反应混合气体各组分的浓度,平衡不移动.
(2)由乙图可知,相同压强温度越高,C%越大,说明升高温度,平衡向正反应移动;
(3)温度相同压强越高,C%越小,说明增大压强,平衡向逆反应移动;
(4)恒温恒容条件下,通入惰性气体,不影响反应混合气体各组分的浓度,平衡不移动.
解答:
解:(1)使用催化剂,加快反应速率,缩短到达平衡的时间,平衡不移动,由图可知,a先到达平衡,故a曲线表示使用催化剂,b曲线表示没有使用催化剂,
故答案为:b;
(2)由乙图可知,相同压强温度越高,C%越大,说明升高温度,平衡向正反应移动,正反应为吸热反应,
故答案为:吸;
(3)温度相同压强越高,C%越小,说明增大压强,平衡向逆反应移动,故x>1+1,即x>2,故答案为:x>2;
(4)恒温恒容条件下,通入惰性气体,不影响反应混合气体各组分的浓度,平衡不移动,C%不变,故答案为:a.
故答案为:b;
(2)由乙图可知,相同压强温度越高,C%越大,说明升高温度,平衡向正反应移动,正反应为吸热反应,
故答案为:吸;
(3)温度相同压强越高,C%越小,说明增大压强,平衡向逆反应移动,故x>1+1,即x>2,故答案为:x>2;
(4)恒温恒容条件下,通入惰性气体,不影响反应混合气体各组分的浓度,平衡不移动,C%不变,故答案为:a.
点评:本题考查化学平衡图象、影响化学平衡的因素,难度中等,注意分析图象中曲线的变化特点,结合平衡移动原理解答.

练习册系列答案
相关题目
原计划实现全球卫星通讯需发射77颗卫星,这与铱(Ir)元素的原子核外电子数恰好相等,因此称为“铱星计划”.已知铱的一种同位素是
Ir,则其中子数与电子数之差是( )
191 77 |
| A、77 | B、114 |
| C、191 | D、37 |
下列各项表达中正确的是( )
A、O2-的结构示意图为: |
| B、Mg2+的电子式:Mg2+ |
C、NaCl的电子式为:Na  |
| D、N2的结构式为::N≡N: |
下列物质属于纯净物的是( )
| A、冰水混合物 | B、洁净的空气 |
| C、食醋 | D、清澈的海水 |
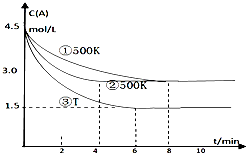 某反应2A(g)?2B(g)+C(g)(吸热反应)在三种不同条件下进行,B、C的起始浓度为0,A的浓度(mol/L)随反应时间(min)的变化情况如图所示.
某反应2A(g)?2B(g)+C(g)(吸热反应)在三种不同条件下进行,B、C的起始浓度为0,A的浓度(mol/L)随反应时间(min)的变化情况如图所示.