题目内容
二氯化二硫(S2Cl2)可用作橡胶工业的硫化剂,常温下它是橙黄色有恶臭的液体,它的分子结构与H2O2相似,熔点为193K,沸点为411K,遇水很容易反应,产生的气体能使品红褪色,S2Cl2可由干燥的氯气通入熔融的硫中制得.下列有关说法不正确的是( )
| A、S2Cl2分子中各原子均达到8电子稳定结构 |
| B、制备S2Cl2的反应是化合反应,不是氧化还原反应 |
| C、S2Cl2遇水反应的化学方程式为:2S2Cl2+2H2O=3S↓+SO2↑+4HCl |
| D、S2Br2与S2Cl2结构相似,熔沸点:S2Br2>S2Cl2 |
考点:氯、溴、碘及其化合物的综合应用
专题:
分析:S2Cl2的分子结构与H2O2相似,熔点为193K,沸点为411K,熔沸点较低,则存在分子,应为共价化合物,对应晶体为分子晶体,S2Cl2的电子式为 ,与水发生2S2Cl2+2H2O=SO2↑+3S↓+4HCl,以此解答该题.
,与水发生2S2Cl2+2H2O=SO2↑+3S↓+4HCl,以此解答该题.
 ,与水发生2S2Cl2+2H2O=SO2↑+3S↓+4HCl,以此解答该题.
,与水发生2S2Cl2+2H2O=SO2↑+3S↓+4HCl,以此解答该题.解答:
解:A.S2Cl2的电子式为  ,分子中各原子均达到8电子稳定结构,故A正确;
,分子中各原子均达到8电子稳定结构,故A正确;
B.S2C12可由干燥的氯气通入熔融的硫中制得,反应中Cl和S的化合价发生了变化,属于氧化还原反应,故B错误;
C.遇水很容易反应,产生的气体能使品红褪色,可知生成SO2,与水发生2S2Cl2+2H2O=SO2↑+3S↓+4HCl,故C正确;
D.S2Br2与S2Cl2结构相似,则相对分子质量越大,沸点越高,所以熔沸点:S2Br2>S2Cl2,故D正确.
故选B.
 ,分子中各原子均达到8电子稳定结构,故A正确;
,分子中各原子均达到8电子稳定结构,故A正确;B.S2C12可由干燥的氯气通入熔融的硫中制得,反应中Cl和S的化合价发生了变化,属于氧化还原反应,故B错误;
C.遇水很容易反应,产生的气体能使品红褪色,可知生成SO2,与水发生2S2Cl2+2H2O=SO2↑+3S↓+4HCl,故C正确;
D.S2Br2与S2Cl2结构相似,则相对分子质量越大,沸点越高,所以熔沸点:S2Br2>S2Cl2,故D正确.
故选B.
点评:本题以S2Cl2的结构为载体,考查分子结构、化学键、氧化还原反应等,难度不大,是对基础知识的综合运用与学生能力的考查,注意基础知识的全面掌握,是一道不错的能力考查题目.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
一般检验SO42-的试剂是( )
| A、BaCl2、稀HNO3 |
| B、AgNO3、稀HNO3 |
| C、稀HCl BaCl2 |
| D、AgNO3 稀HCl |
下列分子中含有手性碳原子的是( )
| A、CF2Cl2 |
| B、CH3CH2OH |
C、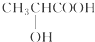 |
| D、CH2═CH-COOH |
将1L含有0.4molCuSO4和0.2molNaCl的水溶液用惰性电极电解,电解一段时间后,在一个电极上增重19.2g,另一个电极上产生气体(标况)的体积是( )
| A、4.48L |
| B、5.6L |
| C、6.72L |
| D、13.44L |
短周期元素X、Y、Z、W 的原子序数依次增大,且原子最外层电子数之和为13,X 的原子半径比Y 的小,X 与W 同主族,Z 是地壳中含量最高的元素.下列说法正确的是( )
| A、由X与Y组成的化合物的沸点总低于由X与Z组成的化合物的沸点 |
| B、元素Z、W 的简单离子的电子层结构不同 |
| C、元素Y 的简单气态氢化物的热稳定性比Z 的强 |
| D、只含X、Y、Z 三种元素的化合物,可能是离子化合物,也可能是共价化合物 |