题目内容
13.0.92g金属钠与水反应后,得100mL溶液,求(1)生成的气体在标准状况下的体积;
(2)反应后所得溶液物质的量浓度.
分析 金属钠与水反应:2Na+2H2O=2NaOH+H2↑,溶质为NaOH,根据方程式计算NaOH、氢气的物质的量,根据V=nVm计算氢气体积,根据c=$\frac{n}{V}$计算溶液的浓度.
解答 解:0.92g金属钠的物质的量为$\frac{0.92g}{23g/mol}$=0.04mol,则:
2Na+2H2O=2NaOH+H2↑
2 2 1
0.04mol n(NaOH) n(H2)
所以n(NaOH)=n(Na)=0.04mol,n(H2)=$\frac{1}{2}$n(Na)=0.02mol,
(1)生成氢气的体积为0.02mol×22.4L/mol=0.448L,
答:氢气的体积为0.448L.
(2)所得NaOH溶液的物质的浓度是$\frac{0.04mol}{0.1L}$=0.4mol/L,
答:所得NaOH溶液的物质的浓度是0.4mol/L.
点评 本题主要考查根据方程式进行的有关计算,旨在考查学生对基础知识的理解掌握,清楚发生的反应是关键.

练习册系列答案
相关题目
3.${\;}_{92}^{235}U$是重要的工业原料,下列说法不正确的是( )
| A. | ${\;}_{92}^{235}U$原子核中含有92个质子 | B. | ${\;}_{92}^{235}U$原子核外有92个电子 | ||
| C. | ${\;}_{92}^{235}U$与${\;}_{92}^{238}U$互称为核素 | D. | ${\;}_{92}^{235}U$与${\;}_{92}^{238}U$中子数不同 |
4.下列关于铁制品腐蚀或保护措施的说法中不正确的有( )
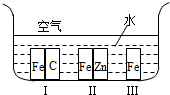

| A. | 在如图所示环境中,铁被腐蚀速率:Ⅰ>Ⅲ>Ⅱ | |
| B. | 军事演习期间给坦克的履带上刷上油漆以防止生锈 | |
| C. | 在海轮的外壳上常焊有锌块,且定期更新 | |
| D. | 将不锈钢制成刀具和餐具,有的刀具还进行烤蓝处理 |
1.用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A. | 标准状况下,22.4L水含有NA个水分子 | |
| B. | 氧气和臭氧的混合物32 g中含有NA个氧原子 | |
| C. | 7.8g Na2O2与水反应时转移0.1NA个电子 | |
| D. | 1.12L氯气中含有NA个氯原子 |
8.比较是化学学习中的一种重要方法.下列各组比较中不正确的是( )
| A. | 在相同条件下的溶解度:NaHCO3>Na2CO3 | |
| B. | 热稳定性:HF>HCl>HBr>HI | |
| C. | 氧化性:F2>Cl2>Br2>I2 | |
| D. | 碳酸钠溶液与稀盐酸互滴时,两种操作现象相同 |
18.下列各项中的两种物质无论以何种比例混合后,只能生成一种含钠化合物的是( )
| A. | Na2CO3、盐酸 | B. | NaOH溶液、CO2 | ||
| C. | NaHCO3溶液、石灰水 | D. | Na2O2、稀硫酸 |