��Ŀ����
15����ҵ�ϳ���FeCl3��Һ��ӡˢ��·�岢��������Ҫ�������£���ʴCu��2FeCl3+Cu=CuCl2+2FeC12��
Ȼ�����Cu��Fe+CuCl2=Cu+FeCl2��
����FeC13��2FeC12+C12=2FeC13��
��ij��·���ϵ�Cu��ʴ��ȫ��ǡ������0.5L2mol/LFeCl3��ȫ���̺�������ı仯��
�ش��������⣺
��1������Clԭ�ӽṹʾ��ͼ��
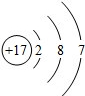 ��
����2����Cu��ʴһ��ʱ����Һ�еĽ����������У�Fe2+��Fe3+��Cu2+����ʱc��Cl-��Ϊ��6mol/L��
��3����ʴ��Cu�������ʵ���Ϊ��0.5mol��
��4������FeC13ʱ����Һ��dz��ɫ���ձ�Ϊ��ɫ�����ĵ�Cl2�ڱ�״���µ��������Ϊ��16.8L��
���� ��1�����ݺ�������Ų�����д��Clԭ�ӽṹʾ��ͼ��
��2������2FeCl3+Cu=CuCl2+2FeC12����Cu��ʴһ��ʱ��������Һ�г�������������з�Ӧ��ʣ�࣬�ݴ˷�����
��3������2FeCl3+Cu=CuCl2+2FeC12����Ͻ�ij��·���ϵ�Cu��ʴ��ȫ��ǡ������0.5L2mol/LFeCl3���㣻
��4����������FeC13��2FeC12+C12=2FeC13����������ת����������ж���Һ��ɫ�仯��������Һ�ж������������������ĵ�Cl2��
��� �⣺��1��Cl��������Ϊ17��ԭ�ӽṹʾ��ͼΪ�� ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��2����Ϊ��ʴCu��2FeCl3+Cu=CuCl2+2FeC12����Cu��ʴһ��ʱ��������Һ�г�������Fe2+��Cu2+�����Fe3+ʣ�࣬��c��Cl-�����伴2mol/L��3=6mol/L��
�ʴ�Ϊ��Fe2+��Fe3+��Cu2+��6��
��3����Ϊ��ʴCu��2FeCl3+Cu=CuCl2+2FeC12����ij��·���ϵ�Cu��ʴ��ȫ��ǡ������0.5L2mol/LFeCl3�����Ը�ʴ��Cu�������ʵ���Ϊ0.5L��2mol/L��$\frac{1}{2}$=0.5mol���ʴ�Ϊ��0.5��
��4������FeC13��2FeC12+C12=2FeC13����������ת�����������������Һ��dz��ɫ���ձ�Ϊ��ɫ�����ݸ�ʴCu��2FeCl3+Cu=CuCl2+2FeC12��
Ȼ�����Cu��Fe+CuCl2=Cu+FeCl2�������ն��������ӵ����ʵ���Ϊ0.5L��2mol/L+0.5L��2mol/L��$\frac{1}{2}$=1.5mol�������ĵ�Cl2�ڱ�״���µ��������Ϊ1.5mol��22.4L/mol=16.8L��
�ʴ�Ϊ��dz�̣��ƣ�16.8��
���� ���⿼��ӡˢ��·�岢������������⣬�ѶȲ�����ȷ�������ʡ����ʷ�Ӧ�����ǽⱾ��ؼ���ע��Ԫ�ػ�����֪ʶ�Ļ��ۣ�

��Ħ���ǹ��ʵ�λ�����߸�����������֮һ����1mol�κ����ʶ�����Լ6.02��1023��ԭ�ӣ���6.02��1023���ǰ����ӵ�����������ԭ�ӵ�Ħ��������1g����HCl��Ħ����������1mol HCl���ӵ���������1mol CO2�к���1mol̼��2mol����
| A�� | �٢ڢ� | B�� | �ڢۢ� | C�� | �ڢܢܢ� | D�� | ȫ�� |
| A�� | ԭ��Һ�п��ܺ���K+��һ��û��HCO3-��OH-������������ɫ����ͨ�����ʯ��ˮ�У�����ʯ��ˮ����� | |
| B�� | ԭ��Һ��һ������Cl-��NO3-�����ܺ���SO42-����Ӧ���ɵ���ɫ���������������ɫ | |
| C�� | ԭ��Һ��������������ΪMg2+��Fe2+������ϡ�����������ķ�ӦΪ3Fe2++4H++NO3-�T3Fe3++NO��+2H2O | |
| D�� | ����ԭ��Һ�м������NaOH��Һ�������ó������ˡ�ϴ�ӡ����յ����أ��õ��Ĺ�������Ϊ107 g |
| ���� | �ݻ�/L | �¶�/�� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min | |
| C��s�� | H2O��g�� | H2��g�� | ||||
| �� | 2 | T1 | 2 | 4 | 3.2 | 2.8 |
| �� | 1 | T2 | 1 | 2 | 1.2 | 3.0 |
��2���ﵽƽ������¶Ⱥ�������䣬����������ٳ���0.8molH2O��3.2molH2�����ʱV��=V��
�����������������=����
��3�����ܱպ��ݵ������У��ܱ�ʾ������Ӧ�ﵽ��ѧƽ��״̬����BD��
A��V����CO2���T2V����H2��
B�����������ܶȱ��ֲ���
C��c��H2O����c��CO2����c��H2��=2��1��2
D����������ƽ����Է����������ֲ���
��4��ijͬѧΪ���о���Ӧ�����Ի�ѧƽ���Ӱ�죬����淴Ӧ������ʱ��Ĺ�ϵ��ͼ��ʾ��
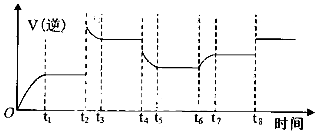
�ɼ���t1��t3��t5��t7ʱ��Ӧ�����˵�ƽ��״̬�����t2��t4��t6��t8ʱ��ֻ�ı���һ����Ӧ��������t6ʱ�̸ı��������ͨ��H2O�����t1��t8�ĸ�ʱ���H2O ��g����ƽ��ת�������t7-t8�����t1��t2���Դ����ơ�����
| A�� | ����������Һ�ֱ���ˮϡ��m��n������Һ��pH�����3����m��n | |
| B�� | ����������Һ�ֱ���������Zn��ȫ��Ӧ��������H2һ���� | |
| C�� | ����������Һ�ֱ����Ũ�ȵ�����������Һǡ�÷�Ӧ����������������Һ�������ͬ | |
| D�� | 1mol/L�������1mol/L�Ĵ���Ļ����Һ������������Һǡ����ȫ��Ӧʱ����Ӧ����Һ��c��CH3COO-��+C��Cl-����c��Na+�� |
 ��ͼΪʵ����ijŨ�����Լ�ƿ�ϵı�ǩ���й����ݣ��Ը��ݱ�ǩ�ϵ��й����ݻش��������⣺
��ͼΪʵ����ijŨ�����Լ�ƿ�ϵı�ǩ���й����ݣ��Ը��ݱ�ǩ�ϵ��й����ݻش��������⣺