题目内容
15.如图图象中,纵坐标为沉淀物的物质的悬,横坐标为向溶液中加入反应物的物质的量,则相应的图象序号与(1)-(4)对应的是BCAD
| 溶液 | 加入物质 | 对应的图象 |
| (1)饱和石灰水 | 通过量CO2气体 | |
| (2)氯化铝溶液 | 加入过量氨水 | |
| (3)MgCl2、AICl3的混合液 | 逐滴加入NaOH溶液至过量 | |
| (4)含少量NaOH的NaAlO2溶液 | 逐滴加入稀盐酸 |
分析 所示图象中,纵坐标为沉淀物的物质的量,横坐标为某溶液中加入反应物的物质的量,
A表示先沉淀至达到最大量,后沉淀部分溶解;
B表示先后加入等量的物质,先沉淀最大量,后沉淀全部溶解;
C表示加入某溶液,沉淀达最大量后,再加入某溶液,沉淀不再增加或溶解;
D表示加入某溶液,经过一段时间后,才出现沉淀,沉淀达最大量后,再加入某溶液,最后沉淀全部溶解.
解答 解:(1)饱和石灰水通过量CO2气体,应先有沉淀:Ca(OH)2+CO2=CaCO3↓+H2O,后沉淀溶解:CaCO3+CO2+H2O=Ca(HCO3)2,两段消耗的CO2气体等量,对照图象应为B;
(2)氨水是弱碱,不能溶解氢氧化铝,氯化铝溶液加入过量氨水的反应方程式为:AlCl3+3NH3•H2O═Al(OH)3↓+3NH4Cl,对照图象应为C;
(3)MgCl2、AlCl3的混合液,逐滴加入NaOH溶液至过量,先是生成氢氧化镁和氢氧化铝沉淀,MgCl2+2NaOH═Mg(OH)2↓+2NaCl;AlCl3+3NaOH═Al(OH)3↓+3NaCl,后是氢氧化铝溶解,Al(OH)3 +NaOH═NaAlO2+2H2O,对照图象应为A;
(4)含少量NaOH的NaAlO2溶液,逐滴加入稀盐酸,先是NaOH和HCl发生中和反应:NaOH+HCl=NaCl+H2O,后是NaAlO2+HCl+H2O=Al(OH)3↓+NaCl,Al(OH)3 +3HCl=AlCl3+3H2O,对照图象应为D;
故答案为:BCAD.
点评 本题考查化学反应与图象的关系,解答本题关键在于理解相关反应,并能熟练写出相应的反应的方程式,并能找出对应的图形即可解题.

练习册系列答案
相关题目
6.将二氧化硫通入到氯化钡溶液中未见到明显现象,把上述溶液分为两份,其中一份a加入NaOH溶液,另一份b中通入Cl2,均有白色沉淀产生,其中a中沉淀的化学式为BaSO3,b中沉淀的化学式为BaSO4.
10.下列材料掺入普通钢中,可形成不锈钢的是( )
| A. | Ni、Cr | B. | Mn、Si | C. | 稀土金属 | D. | W、Pt |
20.纯水不导电,它属于( )
| A. | 强电解质 | B. | 弱电解质 | C. | 非电解质 | D. | 离子化合物 |
7.(1)已知25℃时有关弱酸的电离平衡常数:
①等物质的量浓度的a.CH3COONa、b.NaCN、c.Na2CO3、d.NaHCO3溶液的pH由大到小的顺序为c b d a(填序号).
②25℃时,将20mL 0.1mol•L-1 CH3COOH溶液和20mL 0.1mol•L-1 HSCN溶液分别与20mL 0.1mol•L-1 NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)的变化如图1所示: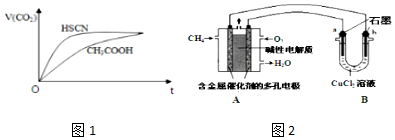
反应初始阶段两种溶液产生CO2气体的速率存在明显差异的原因是HSCN的酸性比CH3COOH强,其溶液中c(H+)较大,故其溶液与NaHCO3溶液的反应速率快.
反应结束后所得两溶液中,c(CH3COO-)<c(SCN-)(填“>”、“<”或“=”)
③若保持温度不变,在醋酸溶液中加入一定量氨气,下列量会变小的是b(填序号).
a.c(CH3COO-)b.c(H+)c.Kw d.醋酸电离平衡常数
(2)甲烷是天然气的主要成分,是生产生活中应用非常广泛的一种化学物质.一定条件下,用甲烷可以消除氮氧化物(NOx)的污染.已知:
CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g);△H1
CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g);△H2
现有一份在相同条件下对H2的相对密度为17的NO与NO2的混合气体,用16g甲烷气体催化还原该混合气体,恰好生成氮气、二氧化碳气体和水蒸气,共放出1042.8kJ热量.
①该混合气体中NO和NO2的物质的量之比为3:1
②已知上述热化学方程式中△H1=-1160kJmol,则△H2=-574 kJ/mol.
③在一定条件下NO气体可以分解为NO2气体和N2气体,写出该反应的热化学方程式4NO(g)=2NO2(g)+N2(g)△H=-293KJ/mol
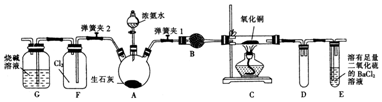
(3)甲烷燃料电池可以提升能量利用率.图2是利用甲烷燃料电池电解50mL2mol/L的氯化铜溶液的装置示意图:
请回答:
①甲烷燃料电池的负极反应式是CH4-8e-+10OH-=CO32-+7H2O
②当A中消耗0.15mol氧气时,B中b极增重6.4g.
| 弱酸化学式 | HSCN | CH3COOH | HCN | H2CO3 |
| 电离平衡常数 | 1.3×10-1 | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7K2=5.6×10-11 |
②25℃时,将20mL 0.1mol•L-1 CH3COOH溶液和20mL 0.1mol•L-1 HSCN溶液分别与20mL 0.1mol•L-1 NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)的变化如图1所示:

反应初始阶段两种溶液产生CO2气体的速率存在明显差异的原因是HSCN的酸性比CH3COOH强,其溶液中c(H+)较大,故其溶液与NaHCO3溶液的反应速率快.
反应结束后所得两溶液中,c(CH3COO-)<c(SCN-)(填“>”、“<”或“=”)
③若保持温度不变,在醋酸溶液中加入一定量氨气,下列量会变小的是b(填序号).
a.c(CH3COO-)b.c(H+)c.Kw d.醋酸电离平衡常数
(2)甲烷是天然气的主要成分,是生产生活中应用非常广泛的一种化学物质.一定条件下,用甲烷可以消除氮氧化物(NOx)的污染.已知:
CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g);△H1
CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g);△H2
现有一份在相同条件下对H2的相对密度为17的NO与NO2的混合气体,用16g甲烷气体催化还原该混合气体,恰好生成氮气、二氧化碳气体和水蒸气,共放出1042.8kJ热量.
①该混合气体中NO和NO2的物质的量之比为3:1
②已知上述热化学方程式中△H1=-1160kJmol,则△H2=-574 kJ/mol.
③在一定条件下NO气体可以分解为NO2气体和N2气体,写出该反应的热化学方程式4NO(g)=2NO2(g)+N2(g)△H=-293KJ/mol
(3)甲烷燃料电池可以提升能量利用率.图2是利用甲烷燃料电池电解50mL2mol/L的氯化铜溶液的装置示意图:
请回答:
①甲烷燃料电池的负极反应式是CH4-8e-+10OH-=CO32-+7H2O
②当A中消耗0.15mol氧气时,B中b极增重6.4g.

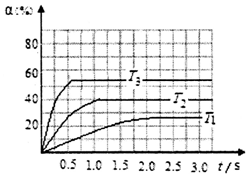 硫及其化合物是重要的化工原料,在工农业生产应用广泛.
硫及其化合物是重要的化工原料,在工农业生产应用广泛.