题目内容
9.已知X、Y、Z中含同种元素,其中X、W是单质且有如图所示的转化关系,则X、W依次为( )
| A. | Fe,Cl2 | B. | C,O2 | C. | N2,O2 | D. | S,O2 |
分析 A、Fe与Cl2反应只能生成FeCl3,FeCl3不与Cl2反应;
B、C与少量O2生成CO,与足量的O2反应生成CO2,CO与O2反应生成CO2,CO2与C反应生成CO;
C、N2不可能一步生成NO2;
D、S与O2不可能一步生成SO3.
解答 解:A、Fe与Cl2反应只能生成FeCl3,FeCl3不与Cl2反应,故A错误;
B、C与少量O2生成CO,CO继续与O2反应生成CO2,CO2与C反应生成CO,C与足量的O2反应生成CO2,故B正确;
C、N2与O2放电生成NO,NO与O2反应生成NO2,但是N2不可能一步生成NO2,故C错误;
D、S与O2只能生成SO2,不可能一步生成SO3,故D错误.
故选B.
点评 本题属于无机推断题,考查了物质间的转化,熟悉相关物质的化学性质是解题关键,注意对相关知识的积累.

练习册系列答案
相关题目
19.钢铁发生析氢腐蚀、吸氧腐蚀时,都发生的电极反应是( )
| A. | 2H++2e-═H2 | B. | Fe-2e-═Fe2+ | ||
| C. | 2H2O+O2+4e-═4OH- | D. | Fe3++e-═Fe2+ |
20.关于符号ZAX2+的判断不正确的是( )
| A. | 它可以表示一个阳离子 | B. | X表示元素的符号 | ||
| C. | Z表示质子数,A则表示质量数 | D. | 此微粒含有电子总数为Z+2 |
4.下列关于化学用语的表示正确的是( )
| A. | 氢氧化钠的电子式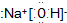 | |
| B. | 质子数为29、中子数为35的铜原子${:}_{29}^{35}$Cu | |
| C. | 氯离子的结构示意图: | |
| D. | 对苯二酚的结构简式: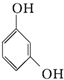 |
14.现有10mL 0.1mol•L-1CH3COOH溶液,下列说法正确的是( )
| A. | 加入10 mL蒸馏水后,CH3COO-的数目减少,c(OH-)增大 | |
| B. | 加入V mL 0.1 mol•L-1 NaOH溶液后,若c(Na+)=c(CH3COO-),则V=10 | |
| C. | 加入10 mL 0.1 mol•L-1NH3•H2O溶液后,溶液中存在:c(CH3COO-)+c(CH3COOH)=c(H+)+c(N${H}_{4}^{+}$) | |
| D. | 将其逐滴加入10 mL 0.1 mol•L-1Na2CO3溶液中,混合溶液中存在:c(H+)+c(CH3COOH)+c(H2CO3)=c(OH-)+c(C${O}_{3}^{2-}$) |
1.实验测得某溶液中仅含有K+、Cu2+、SO42-、Cl-四种离子.,其中K+、Cu2+、Cl-三种离子的个数比为4:5:8,则K+与SO42-的物质的量比为( )
| A. | 4:3 | B. | 4:1 | C. | 2:3 | D. | 2:1 |
18.常温下,下列实验操作所得到的溶液中溶质的物质的量浓度最大的是( )
| A. | 将5.85g氯化钠溶于水形成100mL氯化钠溶液 | |
| B. | 将36.5g氯化氢溶于水形成100mL盐酸 | |
| C. | 将7.45g氯化钾溶于水形成1000mL溶液 | |
| D. | 将9.5g氯化镁溶于水形成1000mL溶液 |
19.混合下列各组物质使之充分反应,加热蒸干产物并在300℃(低于各物质的分解温度)灼烧至质量不变,最终残留固体为纯净物的是( )
| A. | 向亚硫酸钠溶液中滴加过量的溴水 | |
| B. | 将物质的量浓度相等的KAl(SO4)2与Ba(0H)2溶液以体积比1:2混合 | |
| C. | 等体积、等物质的量浓度的碳酸钠与氢氧化钡溶液混合 | |
| D. | 在NaCl溶液中通入过量氟气 |