题目内容
17.将23g单质钠投入含有0.01mol盐酸中,产生氢气的体积在标准状况下是多少?分析 钠的物质的量为1mol,由2Na+2HCl=2NaCl+H2↑,可知HCl不足,故Na还与水发生反应:2Na+2H2O=2NaOH+H2↑,由方程式可知2Na~H2↑,据此计算生成氢气的体积.
解答 解:钠的物质的量为$\frac{23g}{23g/mol}$=1mol,由2Na+2HCl=2NaCl+H2↑,可知HCl不足,故Na还与水发生反应:2Na+2H2O=2NaOH+H2↑,
设生成氢气体积为V,则:
2 Na~H2↑,
2mol 22.4L
1mol V
V=$\frac{22.4L×1mol}{2mol}$=11.2L
答:标况下生成氢气为11.2L.
点评 本题考查化学方程式有关计算,明确发生的反应即可解答,注意酸不足时Na与水反应也生成氢气.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.下列试验中可以用来鉴别乙醇、乙醛、乙酸三种无色液体的是( )
| A. | 浓溴水 | B. | FeCl3溶液 | ||
| C. | 银氨溶液 | D. | 新制的Cu(OH)2悬浊液 |
8.下列化学用语正确的是( )
| A. | HCl的电子式: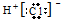 | B. | 氯离子的结构示意图: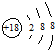 | ||
| C. | 甲烷分子的比例模型: | D. | 核内有8个中子的碳原子:${\;}_{6}^{8}$C |
5.碳原子数为12且只有两个侧链的苯的同系物的同分异构体数目为( )
| A. | 42 | B. | 45 | C. | 48 | D. | 60 |
6.取100mL0.3mol•L-1的H2SO4溶液和300mL0.25mol•L-1的H2SO4溶液配成500mL的溶液所得溶液中H+的物质的量浓度为( )
| A. | 0.265mol•L-1 | B. | 0.525mol•L-1 | C. | 0.21mol•L-1 | D. | 0.42mol•L-1 |
17. 某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如下方案完成实验.
某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如下方案完成实验.
(1)写出实验③中H2O2分解反应方程式并标明电子转移的方向和数目: .
.
(2)实验①和②的目的是探究反应物浓度对反应速率的影响.
实验时由于没有观察到明显现象而无法得出结论.资料显示,通常条件下H2O2稳定,不易分解.为了达到实验目的,你对原实验方案的改进是向反应物中加入等量同种催化剂(或将盛有反应物的试管放在同一热水浴中).
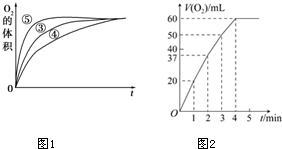
(3)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图1.分析上图能够得出的实验结论:碱性环境能增大H2O2分解的速率;酸性环境能减小H2O2分解速率.
(4)将0.1g MnO2粉末加入50mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图2所示.解释反应速率变化的原因:随着反应的进行,H2O2的浓度减小,反应速率减慢,计算H2O2的初始物质的量浓度为0.11mol/L.(保留两位有效数字,在标准状况下测定)
 某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如下方案完成实验.
某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如下方案完成实验.| 分组实验 | 催化剂 | |
| ① | 10mL 5% H2O2溶液 | 无 |
| ② | 10mL 2% H2O2溶液 | 无 |
| ③ | 10mL 5% H2O2溶液 | 1mL 0.1mol•L-1FeCl3溶液 |
| ④ | 10mL 5%H2O2溶液+少量HCl溶液 | 1mL 0.1mol•L-1FeCl3溶液 |
| ⑤ | 10mL 5% H2O2溶液+少量NaOH溶液 | 1mL 0.1mol•L-1FeCl3溶液 |
 .
.(2)实验①和②的目的是探究反应物浓度对反应速率的影响.
实验时由于没有观察到明显现象而无法得出结论.资料显示,通常条件下H2O2稳定,不易分解.为了达到实验目的,你对原实验方案的改进是向反应物中加入等量同种催化剂(或将盛有反应物的试管放在同一热水浴中).
(3)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图1.分析上图能够得出的实验结论:碱性环境能增大H2O2分解的速率;酸性环境能减小H2O2分解速率.
(4)将0.1g MnO2粉末加入50mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图2所示.解释反应速率变化的原因:随着反应的进行,H2O2的浓度减小,反应速率减慢,计算H2O2的初始物质的量浓度为0.11mol/L.(保留两位有效数字,在标准状况下测定)