题目内容
1.能证明Na2SO3溶液中存在水解平衡SO32-+H2O?HSO3-+OH-的事实是( )| A. | 滴入酚酞溶液变红,再加入H2SO4溶液红色退去 | |
| B. | 滴入酚酞溶液变红,再加入氯水后红色退去 | |
| C. | 滴入酚酞溶液变红,在加入BaCl2溶液后产生沉淀且红色退去 |
分析 如果亚硫酸钠不水解,则溶液中氢氧根离子和氢离子浓度相等,溶液呈中性,向溶液中加入酚酞后溶液不变色,加入和亚硫酸根离子反应的物质后,溶液红色褪色,则证明存在水解平衡,据此进行解答.
解答 A.滴入酚酞试液变红,说明溶液呈碱性,再加入硫酸溶液后,硫酸与亚硫酸钠反应,且硫酸溶液呈酸性,可以时溶液褪色,不能说明存在SO32-+H2O?HSO3-+OH-水解平衡,故A错误;
B.滴入酚酞试液变红,再加入氯水后,氯气和水反应生成盐酸和次氯酸,次氯酸具有漂白性,能使红色褪色,氯气具有强氧化性,Cl2+SO32-+H2O═SO42-+2Cl-+2H+,Cl2+HSO3-+H2O═SO4 2-+2Cl-+3H+,溶液褪色,不能说明存在SO32-+H2O?HSO3-+OH-水解平衡,故B错误;
C.滴入酚酞试液变红,说明溶液中氢氧根离子浓度大于氢离子浓度,再加入氯化钡溶液后,钡离子和亚硫酸根离子反应而和亚硫酸氢根离子不反应,钡离子和亚硫酸根离子反应生成亚硫酸钡沉淀,且溶液红色褪去,所以说明存在SO32-+H2O?HSO3-+OH-水解平衡,故C正确,
故选C;
点评 本题考查盐的水解原理及其应用,题目难度不大,明确盐的水解原理及其影响为解答关键,试题侧重基础知识的考查,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
11.表是元素周期表的一部分,针对表中①一⑨元素,填写下列空白.
(1)④的原子半径比⑤的原于半径大 (填“大”或“小”).
(2)⑧的原子结构示意图为 .
.
(3)①、②、③的非金属性依次增强(填“增强”或“减弱”).
(4)由氢与⑦所形成的化合物的分子式是H2S.
(5)④、⑤和⑥的氧化物对应的水化物中碱性较强的是NaOH(写化学式).
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | |||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(2)⑧的原子结构示意图为
 .
.(3)①、②、③的非金属性依次增强(填“增强”或“减弱”).
(4)由氢与⑦所形成的化合物的分子式是H2S.
(5)④、⑤和⑥的氧化物对应的水化物中碱性较强的是NaOH(写化学式).
12.下列说法正确的是( )
| A. | 最外层电子数等于或大于3(小于8)的元素一定是主族元素 | |
| B. | 元素的气态氢化物越稳定,非金属性越强,其水溶液的酸性越强,还原性越弱 | |
| C. | 在主族元素中,最高正化合价均等于主族序数 | |
| D. | 元素的原子得电子越多,非金属性越强;失电子越多,金属性越强 |
9.某强酸性溶液X中仅含有NH4+、Al3+、Ba2+、Fe2+、Fe3+、CO32-、SO32-、SO42-、Cl-、NO3-中的一种或几种,取该溶液进行连续实验,实验过程如图: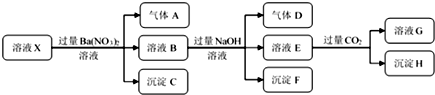
下列有关推断合理的是( )

下列有关推断合理的是( )
| A. | 若要确定溶液X中是否含有Fe3+,其操作为取少量原溶液于试管中,加入适量KSCN溶液,溶液变血红色,则含有Fe3+ | |
| B. | 沉淀C为BaSO4,沉淀H为BaCO3,工业上往BaCO3中加入饱和的Na2CO3可以实现BaSO4的转变 | |
| C. | 溶液中一定含有H+、Al3+、NH4+、Fe2+、SO42-、Cl- | |
| D. | 若溶液X为100 mL,产生的气体A为112 mL(标况),则X中c(Fe2+)=0.05 mol•L-1 |
16.下列叙述中正确的是( )
| A. | 在元素周期表中,零族元素的单质在常温下全部都是气体 | |
| B. | 同周期元素,ⅦA族的原子半径最大 | |
| C. | ⅥA族元素的原子,其半径越大,越容易失去电子 | |
| D. | 所有主族元素的原子形成单原子离子时的最高化合价数都和它的族序数相等 |
6.粗盐中往往含有Ca2+、Mg2+、SO42-,为了有效除去该杂质离子,加入试剂的合理顺序为( )
| A. | 先加NaOH,后加Na2CO3,再加BaCl2 | B. | 先加NaOH,后加BaCl2,再加Na2CO3 | ||
| C. | 先加Na2CO3,后加NaOH,再加BaCl2 | D. | 先加Na2CO3,后加BaCl2,再加NaOH |
13.在相同体积的K2SO4溶液、CuSO4溶液Al2(SO4)3溶液中,分别加入足量的BaCl2溶液,产生相同质量的沉淀,则上述三种溶液的物质的量浓度之比是( )
| A. | 6:3:2 | B. | 3:3:1 | C. | 1:2:3 | D. | 1:1:3 |
10.运用元素周期律分析下面的推断,其中错误的是( )
| A. | 硼的氧化物的水化物可能具有两性 | |
| B. | 砹(At)为有色固体,HAt不稳定,AgAt见光容易分解,但不溶于水也不溶于稀酸 | |
| C. | 氢氧化铷(RbOH)易溶于水 | |
| D. | 硒化氢(H2Se)是无色、有毒、比H2S稳定的气体 |