题目内容
9.某强酸性溶液X中仅含有NH4+、Al3+、Ba2+、Fe2+、Fe3+、CO32-、SO32-、SO42-、Cl-、NO3-中的一种或几种,取该溶液进行连续实验,实验过程如图: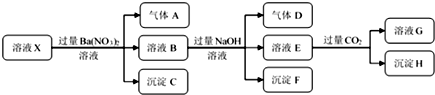
下列有关推断合理的是( )
| A. | 若要确定溶液X中是否含有Fe3+,其操作为取少量原溶液于试管中,加入适量KSCN溶液,溶液变血红色,则含有Fe3+ | |
| B. | 沉淀C为BaSO4,沉淀H为BaCO3,工业上往BaCO3中加入饱和的Na2CO3可以实现BaSO4的转变 | |
| C. | 溶液中一定含有H+、Al3+、NH4+、Fe2+、SO42-、Cl- | |
| D. | 若溶液X为100 mL,产生的气体A为112 mL(标况),则X中c(Fe2+)=0.05 mol•L-1 |
分析 在强酸性溶液中一定不会存在CO32-、SO32-离子;加入过量硝酸钡生成沉淀,则该沉淀C为BaSO4,说明溶液中含有SO42-离子,生成气体A,则A只能是NO,说明溶液中含有还原性离子,则一定为Fe2+离子,溶液B中加入过量NaOH溶液,沉淀F只为Fe(OH)3,生成气体D,则D为NH3,说明溶液中含有NH4+离子;溶液E中通入CO2气体,生成沉淀H,则H为Al(OH)3,E为NaOH和NaAlO2,说明溶液中含有Al3+离子,再根据离子共存知识,溶液中含有Fe2+离子,则一定不含NO3-离子和SO32-离子,那么一定含有SO42-离子,那么就一定不含Ba2+离子,不能确定是否含有的离子Fe3+和Cl-,以此进行解答.
解答 解:依据分析可知:溶液中一定存在:NH4+、Al3+、Fe2+、SO42-,一定不含有:Ba2+、CO32-、SO32-、NO3-,不能确定是否含有:Fe3+和Cl-,
A、根据上述连续实验不能确定溶液X中是否含有Fe3+,若要确定溶液X中是否含有Fe3+,其操作为取少量原溶液于试管中,加入适量KSCN溶液,溶液变血红色,则含有Fe3+,故A正确;
B、根据上述分析可知沉淀C为BaSO4,H为Al(OH)3,BaCO3与过量的二氧化碳生成碳酸氢钡,易溶于水,故B错误;
C、依据分析可知,溶液中一定存在:NH4+、Al3+、Fe2+、SO42-,不能确定Cl-是否存在,故C错误;
D、生成气体A的离子反应方程式为:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,产生的气体A为112 mL,物质的量为:$\frac{0.112L}{22.4L/mol}$=0.005mol,故n(Fe2+)=3×0.005=0.015mol,c(Fe2+)=$\frac{0.015mol}{0.1L}$=0.15mol/L,故D错误,
故选A.
点评 本题考查了常见阴阳离子的检验、无机推断,题目难度中等,注意掌握常见离子的性质及检验方法,试题充分考查了学生的分析、理解能力及灵活应用所学知识的能力.

| A. | Ca | B. | Li | C. | K | D. | Na |
| A. | 一定条件下与氢气反应 | B. | 与足量的液溴反应 | ||
| C. | 在导管口点燃 | D. | 通入足量溴水中 |
| A. | 酸性:HF>HCl>H2S | B. | 沸点:CBr4>CCl4>CF4 | ||
| C. | 碱性:Ca(OH)2>Mg(OH)2>Al(OH)3 | D. | 稳定性:H2O>H2S>H2Se |
| A. | 滴入酚酞溶液变红,再加入H2SO4溶液红色退去 | |
| B. | 滴入酚酞溶液变红,再加入氯水后红色退去 | |
| C. | 滴入酚酞溶液变红,在加入BaCl2溶液后产生沉淀且红色退去 |
| A. | 烯烃官能团的结构式:C=C | B. | 醛基的结构简式:HOC- | ||
| C. | 氢分子中共用电子对的轨道表示: | D. | 丙酸的结构简式:COOHCH2CH3 |
| A. | CO和N2 | B. | O3和SO2 | C. | N2H4和C2H4 | D. | CO2和N2O |
 .
. .
.
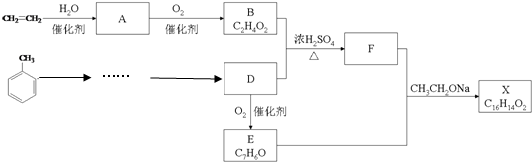
 到D的合成路线(无机试剂任选,用合成路线流程图表示).
到D的合成路线(无机试剂任选,用合成路线流程图表示).