题目内容
12.已知A、B、C、D的原子序数都不超过18,.它们的离子aA(n+1)+、bBn+、cC(n+1)-、dDn- 均具有相同的电子层结构,则下列叙述正确的是( )| A. | 原子序数:a>b>c>d | B. | 离子半径:A(n+1)+>Bn+>C(n+1)->Dn- | ||
| C. | 原子半径:A>B>C>D | D. | 单质还原性:B>A,单质氧化性:D>C |
分析 已知aA(n+1)+、bBn+、cC(n+1)-、dDn-均具有相同的电子层结构,则有:a-n-1=b-n=c+n+1=d+n,则有A、B在周期表中C、D的下一周期,并且原子序数:a>b>d>c,结合元素周期律递变规律解答该题.
解答 解:A.aA(n+1)+、bBn+、cC(n+1)-、dDn-均具有相同的电子层结构,则有:a-n-1=b-n=c+n+1=d+n,则有A、B在周期表中C、D的下一周期,并且原子序数:a>b>d>c,故A错误;
B.具有相同电子层结构的离子,原子序数大的离子半径小,则离子半径为C(n+1)->Dn->Bn+>A(n+1)+,故B错误;
C.同周期元素从左到右原子半径逐渐减小,核外电子层数越多,原子半径越大,则原子半径B>A>C>D,故C错误;
D.同周期从左向右金属的还原性减弱,单质的氧化性增强,则单质还原性为B>A,单质氧化性为D>C,故D错误.
故选D.
点评 本题考查位置结构性质的相互关系及应用,侧重于学生的分析能力的考查,明确核外电子排布确定元素所在周期表中的位置以及把握元素周期律的递变规律是解答该题的关键,题目难度不大.

练习册系列答案
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南大学出版社系列答案
同步练习西南大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目
20. 离子液体在有机合成、无机合成等方面有着重要应用.咪唑是合成“离子液体”的一种原料,其结构如图所示,下列有关咪唑说法正确的是( )
离子液体在有机合成、无机合成等方面有着重要应用.咪唑是合成“离子液体”的一种原料,其结构如图所示,下列有关咪唑说法正确的是( )
 离子液体在有机合成、无机合成等方面有着重要应用.咪唑是合成“离子液体”的一种原料,其结构如图所示,下列有关咪唑说法正确的是( )
离子液体在有机合成、无机合成等方面有着重要应用.咪唑是合成“离子液体”的一种原料,其结构如图所示,下列有关咪唑说法正确的是( )| A. | 分子式为C3H3N2 | |
| B. | 分子中含有一种非极性键和两种极性键 | |
| C. | 可以发生取代、加成、氧化反应 | |
| D. | 一氯取代物的同分异构体共有5种 |
7.不溶于水且比水轻的一组液体是( )
| A. | 甲苯、四氯化碳 | B. | 硝基苯、二氯甲烷 | C. | 己烯、苯 | D. | 酒精、溴 |
17.下列属于同分异构体的一组是( )
| A. | ${\;}_{1}^{1}$H和${\;}_{1}^{3}$H | B. | O2和O3 | C. | 正丁烷和异丁烷 | D. | 乙烯和丙烯 |
4.把3mol铜粉投入含4mol硝酸和1mol硫酸的稀溶液中,则放出的气体(假设气体全为NO)的物质的量为( )
| A. | 1mol | B. | 1.5mol | C. | 2mol | D. | 2.5mol |
1.下列实验能获得成功的是( )
| A. | 将乙醛滴入银氨溶液中,加热煮沸制银镜 | |
| B. | 苯与溴水反应制取溴苯 | |
| C. | 向少量苯酚稀溶液中逐滴加入饱和溴水,边加边振荡,观察沉淀 | |
| D. | 1mol•L-1CuSO4溶液2mL和0.5mol•L-1NaOH溶液4mL混合后加入40%的乙醛溶液0.5mL,加热煮沸观察沉淀的颜色 |
2.下列反应属于吸热反应的是( )
| A. | 金属钠与水反应 | B. | 化石燃料的燃烧 | ||
| C. | 氢氧化钡晶体与氯化铵晶体混合 | D. | 氢氧化钠与盐酸反应 |
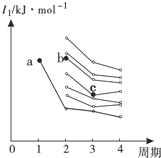 图是部分主族元素第一电离能梯度图,图中a点对应的元素为氢,b、c两点对应的元素分别为O、Si(填元素符号).
图是部分主族元素第一电离能梯度图,图中a点对应的元素为氢,b、c两点对应的元素分别为O、Si(填元素符号).