题目内容
 某离子晶体的晶胞结构如图所示,X(
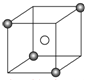
某离子晶体的晶胞结构如图所示,X( )位于立方体的顶点,Y(○)位于立方体的中心.试分析:
)位于立方体的顶点,Y(○)位于立方体的中心.试分析:(1)晶体中每个Y同时吸引
(2)该晶体的化学式为
考点:离子化合物的结构特征与性质,晶胞的计算
专题:
分析:由离子晶体晶胞图,X位于立方体的顶点,Y位于立方体中心,则1个晶胞中含X为4×
=
,含Y为1,X、Y的离子个数之比为1:2,1个Y与4个X形成空间正四面体结构,以此来解答.
| 1 |
| 8 |
| 1 |
| 2 |
解答:
解:(1)从晶胞结构图中可直接看出,每个Y同时吸引4个X,故答案为:4;
(2)在晶胞中,平均包含X数为4×
=
,平均包含Y数为1,所以在晶体中X和Y的个数之比为1:2,晶体的化学式为XY2或Y2X,故答案为:XY2或Y2X.
(2)在晶胞中,平均包含X数为4×
| 1 |
| 8 |
| 1 |
| 2 |
点评:本题考查晶胞计算,注意X、Y的位置及均摊法计算是解答本题的关键,学生需具有一定的空间想象能力,题目难度中等.

练习册系列答案
相关题目
下列物质中,不能通过化合反应直接生成的是( )
| A、FeS |
| B、Fe(OH)3 |
| C、FeCl2 |
| D、Al(OH)3 |
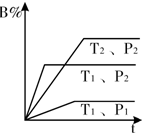 已知某可逆反应mA(g)+n B(g)?pC(g)△Η=Q在密闭容器中进行,如图中表示在不同反应时间t时,温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线,由曲线分析下列判断正确的( )
已知某可逆反应mA(g)+n B(g)?pC(g)△Η=Q在密闭容器中进行,如图中表示在不同反应时间t时,温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线,由曲线分析下列判断正确的( )| A、T1<T2 P1>P2 m+n>p Q<0 |
| B、T1>T2 P1<P2 m+n>p Q<0 |
| C、T1<T2 P1>P2 m+n<p Q>0 |
| D、T1>T2 P1<P2 m+n<p Q>0 |
氧化还原反应广泛地存在于生产和生活之中.下列过程中不涉及氧化还原反应的是( )
| A、金属的冶炼 | B、燃放鞭炮 |
| C、食物的腐败 | D、豆浆制豆腐 |
下列说法正确的是( )
| A、1molCO2在20℃是的体积大于22.4L |
| B、1molCO2和1molCO的体积相同 |
| C、1molCO2与38gCO所含分子数相同 |
| D、1molCO2在标准状况下的体积约为22.4L |
将2.32g Na2CO3、NaOH的固体混合物完全溶解于水,制成溶液,然后向该溶液中逐滴加入1mol/L的盐酸,所加盐酸的体积与产生CO2的体积(标准状况)关系如下图所示,下列说法中错误的是( )
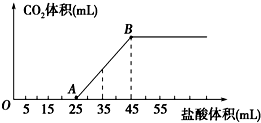

| A、OA段发生反应的离子方程式为:H++OH-═H2O CO32-+H+═HCO3- |
| B、当加入35mL盐酸时,产生CO2的体积为224mL |
| C、A点溶液中的溶质为NaC1、NaHCO3 |
| D、混合物中NaOH的质量0.60g |
 空气中CO2浓度的持续走高已经引起人们的高度重视,科学家们指出大气中二氧化碳的持续上升不仅会使全球变暖,还会对全球,改变着海水中溶解的无机碳(CO2、HCO3-、CO32-)的浓度与比例.中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%.
空气中CO2浓度的持续走高已经引起人们的高度重视,科学家们指出大气中二氧化碳的持续上升不仅会使全球变暖,还会对全球,改变着海水中溶解的无机碳(CO2、HCO3-、CO32-)的浓度与比例.中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%.