题目内容
将2.32g Na2CO3、NaOH的固体混合物完全溶解于水,制成溶液,然后向该溶液中逐滴加入1mol/L的盐酸,所加盐酸的体积与产生CO2的体积(标准状况)关系如下图所示,下列说法中错误的是( )
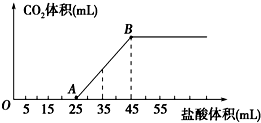

| A、OA段发生反应的离子方程式为:H++OH-═H2O CO32-+H+═HCO3- |
| B、当加入35mL盐酸时,产生CO2的体积为224mL |
| C、A点溶液中的溶质为NaC1、NaHCO3 |
| D、混合物中NaOH的质量0.60g |
考点:化学方程式的有关计算,有关混合物反应的计算
专题:计算题
分析:A、OA段发生反应的离子方程式为:H++OH-═H2O CO32-+H+═HCO3-;
B、AB段发生反应的离子方程式为:HCO3-+H+=H2O+CO2↑,根据方程式来求解;
C、OA段发生反应的离子方程式为:H++OH-═H2O CO32-+H+═HCO3-,所以A点的溶质为NaC1、NaHCO3;
D、根据AB段求出二氧化碳的物质的量,然后根据碳守恒求出碳酸钠的质量,最后根据总质量求氢氧化钠的质量.
B、AB段发生反应的离子方程式为:HCO3-+H+=H2O+CO2↑,根据方程式来求解;
C、OA段发生反应的离子方程式为:H++OH-═H2O CO32-+H+═HCO3-,所以A点的溶质为NaC1、NaHCO3;
D、根据AB段求出二氧化碳的物质的量,然后根据碳守恒求出碳酸钠的质量,最后根据总质量求氢氧化钠的质量.
解答:
解:A、OA段发生反应的离子方程式为:H++OH-═H2O CO32-+H+═HCO3-,故A正确;
B、AB段发生反应的离子方程式为:HCO3-+H+=H2O+CO2↑,根据方程式n(CO2)=(35-25)×10-3L×1mol/L=0.01mol,所以二氧化碳的体积为:0.01mol×22.4L/mol=224mL,故B正确;
C、OA段发生反应的离子方程式为:H++OH-═H2O CO32-+H+═HCO3-,所以A点的溶质为NaC1、NaHCO3,故C正确;
D、由反应HCO3-+H+=H2O+CO2↑,n(CO2)=n(Na2CO3)=(45-25)×10-3×1=0.02mol,所以氢氧化钠的质量为2.32g-0.02×106g=0.2g,故D错误;
故选D.
B、AB段发生反应的离子方程式为:HCO3-+H+=H2O+CO2↑,根据方程式n(CO2)=(35-25)×10-3L×1mol/L=0.01mol,所以二氧化碳的体积为:0.01mol×22.4L/mol=224mL,故B正确;
C、OA段发生反应的离子方程式为:H++OH-═H2O CO32-+H+═HCO3-,所以A点的溶质为NaC1、NaHCO3,故C正确;
D、由反应HCO3-+H+=H2O+CO2↑,n(CO2)=n(Na2CO3)=(45-25)×10-3×1=0.02mol,所以氢氧化钠的质量为2.32g-0.02×106g=0.2g,故D错误;
故选D.
点评:本题考查混合物计算,理解判断各阶段发生的反应是关键,侧重学生分析判断和计算能力的考查,难度中等.

练习册系列答案
相关题目
下列描述中正确的是( )
| A、需要加热才能发生的反应一定是吸热反应 |
| B、中和反应都是放热反应 |
| C、放热反应的反应速率总是大于吸热反应的反应速率 |
| D、同温同压下,反应H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H不同 |
下列各组物质的性质比较中不正确的是( )
| A、酸性:HClO4>H2SO4>H3 PO4 |
| B、热稳定性:SiH4>PH3>H2 S |
| C、碱性:NaOH>Mg(OH)2>Al(OH)3 |
| D、氧化性:F2>C12>Br2 |
下列离子方程式中,正确的是( )
| A、稀硫酸与氢氧化钡溶液反应:Ba2++SO42-?BaSO4↓ |
| B、稀盐酸滴在铜片上:Cu+2H+?Cu2++H2↑ |
| C、小苏打与氢氧化钠溶液混合:HCO3-+OH-?CO2↑+H2O |
| D、氧化铜与稀硫酸混合:CuO+2H+?Cu2++H2O |
甲、乙、丙3个烧杯中分别装有稀H2SO4、CuCl2溶液、饱和食盐水,甲中电极为锌片和铜片,乙中电极为石墨棒C1、C2,丙中电极为石墨棒C3、铁片,电极之间用导线相连.则下列叙述不正确的是( )


| A、甲是化学能转变为电能,乙、丙是电能转变为化学能 |
| B、C1、C2分别是阳极、阴极,锌片、C3上都发生氧化反应 |
| C、C1和C3放出的气体相同,铜片和铁片放出的气体也相同 |
| D、甲中溶液的pH逐渐升高,乙、丙中溶液的pH逐渐减小 |
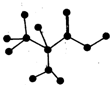 如图是某有机物分子中C、H、O、N四种原子的成键方式示意图(短线表示单键或者双键).下列关于该有机物的说法正确的是.
如图是某有机物分子中C、H、O、N四种原子的成键方式示意图(短线表示单键或者双键).下列关于该有机物的说法正确的是.| A、在一定条件下,可以通过聚合反应生成高分子化合物 |
| B、分子式为C3H6NO2 |
| C、能和NaOH溶液反应,但不能和盐酸溶液反应 |
| D、不能和NaHCO3溶液反应生成CO2 |
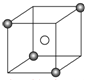 某离子晶体的晶胞结构如图所示,X(
某离子晶体的晶胞结构如图所示,X( )位于立方体的顶点,Y(○)位于立方体的中心.试分析:
)位于立方体的顶点,Y(○)位于立方体的中心.试分析: