题目内容
下列物质的用途中,利用了物质的氧化性的是( )
| A、用漂白粉消毒游泳池中的水 |
| B、用稀盐酸除去热水瓶胆壁上的水垢(主要成分是CaCO3) |
| C、用食盐腌渍食物 |
| D、用小苏打治疗胃酸过多 |
考点:氧化还原反应,重要的氧化剂
专题:
分析:利用物质的氧化性,说明该物质在反应中得电子而作氧化剂,据此分析解答.
解答:
解:A.漂白粉具有强氧化性,能将蛋白质氧化而杀菌消毒,所以利用物质的氧化性,故A正确;
B.CaCO3+2HCl=CaCl2+CO2↑+H2O,该反应中没有电子转移,不属于氧化还原反应,属于复分解反应,故B错误;
C.利用盐溶解使食物和食物所处的环境中的钠离子和氯离子浓度升高,使食物不易变质,不属于氧化还原反应,故C错误;
D.NaHCO3+HCl=NaCl+CO2↑+H2O,该反应中没有电子转移,不属于氧化还原反应,属于复分解反应,故D错误;
故选A.
B.CaCO3+2HCl=CaCl2+CO2↑+H2O,该反应中没有电子转移,不属于氧化还原反应,属于复分解反应,故B错误;
C.利用盐溶解使食物和食物所处的环境中的钠离子和氯离子浓度升高,使食物不易变质,不属于氧化还原反应,故C错误;
D.NaHCO3+HCl=NaCl+CO2↑+H2O,该反应中没有电子转移,不属于氧化还原反应,属于复分解反应,故D错误;
故选A.
点评:本题考查氧化还原反应,侧重考查化学与生活,明确反应原理即可解答,注意把握氧化还原反应特征,题目难度不大.

练习册系列答案
相关题目
水溶液X中只可能溶有K+、Mg2+、Al3+、[Al(OH)4]-、SiO32-、CO32-、SO32-、SO42-中的若干种离子.某同学对该溶液进行了如下实验:下列判断正确的是( )
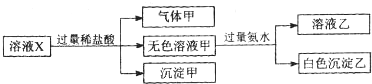

| A、气体甲一定是纯净物 |
| B、沉淀甲是硅酸和硅酸镁的混合物 |
| C、K+、[Al(OH)4]-和SiO32-一定存在于溶液X中 |
| D、CO32-和SO42-一定不存在于溶液X中 |
下列变化过程中,只破坏共价键的是( )
| A、冰变水 |
| B、将Na2SO4熔融呈液态 |
| C、HCl溶于水得盐酸 |
| D、从NH4HCO3中闻到了刺激性气味 |
一氧化碳与氢气在催化剂作用下合成甲醇的反应为:CO(g)+2H2 (g)?CH3OH(g).在容积均为1L的a、b、c、d、e5个密闭容器中分别充入1mol CO和2mol H2等量混合气体,控温.实验测得相关数据如图(1、2),温度分别为300℃、500℃的密闭容器中,甲醇的物质的量与时间的关系;温度分别为T1~T5的密闭容器中,反应均进行到5min时甲醇的体积分数.下列有关说法正确的是( )


| A、K1<K2 |
| B、该反应的正反应是气体体积减小的吸热反应 |
| C、将容器c中的平衡态转变到容器d中的平衡态,可采取的措施有升温或减压 |
| D、反应到5min时,a、b两容器中平衡正向移动,d、e两容器中平衡逆向移动 |
已知X、Z、M、W是短周期中的四种元素,且Z、M、W原子序数依次增大,Ne与Wn-的电子数相同.X元素原子形成的离子是一个质子,Z的单质在常温下是无色气体且Z原子的单电子个数是同周期元素原子中最多的.下面有关推测不正确的是( )
| A、ZO3-的空间构型是平面三角形 |
| B、Z、M、W三种元素的第一电离能由大到小的顺序是W>M>Z |
| C、W所在族的氢化物中沸点最低的是HCl |
| D、在ZX4W中,各种粒子间的相互作用力包括极性共价键、配位键、离子键 |
下列有关卤族元素的叙述不正确的是( )
| A、卤素单质从F2到I2,颜色加深,熔沸点升高 |
| B、卤族元素从Cl到I,最高价氧化物对应水化物的酸性减弱 |
| C、卤族元素从F到I,HX水溶液酸性增强 |
| D、卤素单质氧化性F2>Cl2>Br2>I2,因此排在前面的卤素单质可将排在后面的卤素从它的盐溶液中置换出来 |
根据如图结合电化学原理,分析判断下列叙述中不正确的是( )


| A、若向烧杯a中滴加几滴酚酞试液,溶液呈红色 |
| B、装置工作过程中,烧杯b中电极发生氧化反应 |
| C、烧杯c的左侧的电极反应为2H2O+2e-=2OH-+H2↑ |
| D、烧杯c的右侧溶液由黄色变为橙色,是因为该侧电极上发生了反应2CrO42-+H2O-2e-=Cr2O72-+2OH- |
 超细碳酸钙,粒径范围为1-100nm,其应用非常广泛.下图为某化工企业生产超细碳酸钙的原理
超细碳酸钙,粒径范围为1-100nm,其应用非常广泛.下图为某化工企业生产超细碳酸钙的原理