题目内容
单质铁溶于一定浓度的硝酸溶液中反应的离子方程式为:aFe+bNO3-+cH+=dFe2++fFe3++gNO↑+hNO2↑+kH2O.下列关系一定成立的是( )
| A、2d+3f-b+c=0 |
| B、2d+3f-3g-h=0 |
| C、4b-2h-c=0 |
| D、若d:f=1,则g:h=1 |
考点:氧化还原反应方程式的配平,离子方程式的书写
专题:氧化还原反应专题
分析:依据N原子个数守恒可知:b=g+h;
依据铁原子个数守恒可知:a=d+f;
依据氧原子个数守恒可知:3b=g+k+2h;
依据氢原子个数守恒可知:c=2k;
依据电荷守恒可知:c×1-1×b=3f+2d;
依据得失电子守恒可知:d×2+f×3=3g+h,据此解答.
依据铁原子个数守恒可知:a=d+f;
依据氧原子个数守恒可知:3b=g+k+2h;
依据氢原子个数守恒可知:c=2k;
依据电荷守恒可知:c×1-1×b=3f+2d;
依据得失电子守恒可知:d×2+f×3=3g+h,据此解答.
解答:
解:A.依据电荷守恒可知:c×1-1×b=3f+2d,即:3f+2d+b-c=0,故A错误;
B.铁做还原剂被氧化为Fe2+、Fe3+,硝酸根做氧化剂被还原为NO、NO2,根据得失电子相等,所以d×2+f×3=3g+h,即:2d+3f-3g-h=0,故B正确;
C.依据N原子个数守恒可知:b=g+h;依据氧原子个数守恒可知:3b=g+k+2h;依据氢原子个数守恒可知:c=2k;所以3b=b-h+
+2h,即:4b-2h-c=0,故C正确;
D.依据得失电子守恒可知:d×2+f×3=3g+h,若d=f,则5d=3g+h,不能由此推出g=h,故D错误;
故选:BC.
B.铁做还原剂被氧化为Fe2+、Fe3+,硝酸根做氧化剂被还原为NO、NO2,根据得失电子相等,所以d×2+f×3=3g+h,即:2d+3f-3g-h=0,故B正确;
C.依据N原子个数守恒可知:b=g+h;依据氧原子个数守恒可知:3b=g+k+2h;依据氢原子个数守恒可知:c=2k;所以3b=b-h+
| c |
| 2 |
D.依据得失电子守恒可知:d×2+f×3=3g+h,若d=f,则5d=3g+h,不能由此推出g=h,故D错误;
故选:BC.
点评:本题考查了氧化还原反应规律,侧重考查得失电子数、原子个数守恒规律,题目难度中等.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
由苯乙烯和羟基乙酸乙酯(HO-CH2-COOCH2CH3)组成的混合物中,若碳元素的质量分数为70%,那么氢元素的质量分数约为( )
| A、4.6% | B、7.7% |
| C、15.6% | D、无法计算 |
用浓H2SO4跟分子式分别为C2H6O和C3H8O的醇的混合液反应,可得到醚的种类有( )
| A、1种 | B、3种 | C、5种 | D、6种 |
某一元醛发生银镜反应,生成金属银4.32g,等量该醛完全燃烧后,可生成水1.08g.则此醛可以是下列中的( )
| A、丙醛 | B、丙烯醛 | C、丁醛 | D、乙醛 |

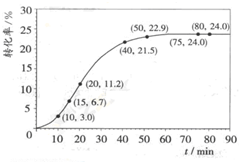 甲酸甲酯水解反应方程式为:HCOOCH3(l)+H2O(l)?HCOOH(l)+CH3OH(l);△H>0
甲酸甲酯水解反应方程式为:HCOOCH3(l)+H2O(l)?HCOOH(l)+CH3OH(l);△H>0 单体,则A中含有的官能团是
单体,则A中含有的官能团是