题目内容
13.下列关于化学键的叙述,正确的是( )| A. | 离子化合物中一定含有离子键 | |
| B. | 单质分子中均存在化学键 | |
| C. | 含有金属元素的物质中均存在离子键 | |
| D. | 含有共价键的化合物一定是共价化合物 |
分析 化学键包括离子键、共价键和金属键,离子化合物中一定含有离子键,可能含有共价键,共价化合物中只含共价键,一定不含离子键,以此解答该题.
解答 解:A.含有离子键的化合物为离子化合物,则离子化合物中一定含有离子键,故A正确;
B.如为单原子分子,则不存在化学键,故B错误;
C.含有金属元素的化合物不一定含有离子键,为AlCl3,为共价化合物,故C错误;
D.离子化合物中一定含有离子键,可能含有共价键,如KOH,则含有共价键的化合物不一定是共价化合物,故D错误.
故选A.
点评 本题考查化合物和化学键的关系,为高频考点,明确共价化合物和离子化合物的概念是解本题关键,注意二者的区别,难度不大.

练习册系列答案
相关题目
3.已知元素的原子序数,可以推知原子的①中子数 ②核电荷数 ③核外电子数 ④在周期表中的位置,其中正确的是( )
| A. | ①③ | B. | ②③ | C. | ①②③ | D. | ②③④ |
1.萘( )是最简单的稠环芳香烃.下列关于萘的说法中正确的是( )
)是最简单的稠环芳香烃.下列关于萘的说法中正确的是( )
 )是最简单的稠环芳香烃.下列关于萘的说法中正确的是( )
)是最简单的稠环芳香烃.下列关于萘的说法中正确的是( )| A. | 萘与足量氢气充分加成的产物一氯代物有2种 | |
| B. | 1mol萘最多可与6mol H2加成 | |
| C. | 萘的一氯代物有2种,二氯代物有10种 | |
| D. | 萘属于苯的同系物 |
5.如图为周期表中短周期的一部分,若X原子最外层电子数比次外层电子数少3,则下列说法正确的是( )
| R | ||
| X | Y | Z |
| A. | X的氢化物比R的氢化物稳定 | |
| B. | 原子半径大小顺序是Z>Y>X>R | |
| C. | Z的单质能与Y的某些化合物发生置换反应 | |
| D. | R的最高价氧化物对应水化物分子为HRO3或H3RO4 |
2.将一定质量的镁铜合金加入到100mL某浓度HNO3中,两者恰好反应,假设反应的还原产物只有NO气体.反应后向所得溶液中加入物质的量浓度为3mol/L的NaOH溶液至沉淀完全,测得生成沉淀质量比原合金质量增加5.1g;则下列有关叙述中不正确的是( )
| A. | 开始加入合金的总物质的量为0.15mol | |
| B. | 生成NO气体体积在标准状况下为2.24L | |
| C. | 生成沉淀完全时消耗NaOH溶液体积为100mL | |
| D. | 原硝酸物质的量浓度为1mol/L |
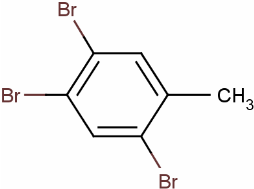 +3HBr.
+3HBr.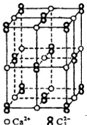 碳族元素的单质及其化合物是一类重要物质.请回答下列问题:
碳族元素的单质及其化合物是一类重要物质.请回答下列问题: ,其中碳氧原子之间共价键是c(填序号).
,其中碳氧原子之间共价键是c(填序号).