题目内容
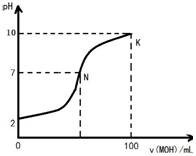 常温下,向100mL 0.01mol?L-1盐酸中逐滴加入0.02mol?L-1 MOH溶液,如图所示,曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计).下列说法中不正确的是( )
常温下,向100mL 0.01mol?L-1盐酸中逐滴加入0.02mol?L-1 MOH溶液,如图所示,曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计).下列说法中不正确的是( )| A、MOH是弱碱 | ||
| B、N点c(Cl-)=c(M+) | ||
C、随着MOH溶液的滴加,比值
| ||
| D、K点对应的溶液c(MOH)+c(OH-)-c(H+)=0.001mol?L-1 |
考点:酸碱混合时的定性判断及有关ph的计算
专题:电离平衡与溶液的pH专题
分析:0.01mol?L-1 HA溶液中pH=2,则HA是强酸,N点时溶液呈中性,当加入MOH100mL时,碱剩余若是强碱,则pH将会大于10,但是此时pH=10,所以MOH是弱碱,根据物料守恒计算K点c(MOH)和c(M+)的和.
解答:
解:A.0.01mol?L-1 HA溶液中pH=2,则HA是强酸,当加入MOH100mL时,碱剩余若是强碱,则pH将会大于10,但是此时pH=10,所以MOH是弱碱,故A正确;
B.N点时溶液呈中性,根据电荷守恒:c(Cl-)+c(OH-)=c(M+)+c(H+),c(OH-)=c(H+),所以c(Cl-)=c(M+),故B正确;
C.比值
=K,不随着物质的量的变化而变化,故C正确;
D.在K点时混合溶液体积是碱溶液的2倍,根据物料守恒结合溶液体积变化知,c(MOH)+c(M+)=0.01mol?L-1,根据电荷守恒得c(M+)+c(H+)=c(OH-)+c(Cl-),c(MOH)+c(OH-)-c(H+)=c(M+)-c(Cl-)+c(MOH)=0.01mol?L-1-0.005mol?L-1=0.005mol?L-1,故D错误;
故选D.
B.N点时溶液呈中性,根据电荷守恒:c(Cl-)+c(OH-)=c(M+)+c(H+),c(OH-)=c(H+),所以c(Cl-)=c(M+),故B正确;
C.比值
| c(M+)?c(OH-) |
| c(MOH) |
D.在K点时混合溶液体积是碱溶液的2倍,根据物料守恒结合溶液体积变化知,c(MOH)+c(M+)=0.01mol?L-1,根据电荷守恒得c(M+)+c(H+)=c(OH-)+c(Cl-),c(MOH)+c(OH-)-c(H+)=c(M+)-c(Cl-)+c(MOH)=0.01mol?L-1-0.005mol?L-1=0.005mol?L-1,故D错误;
故选D.
点评:本题考查了酸碱混合时的定性判断,注意根据酸溶液的pH和酸的浓度确定酸的强弱,为易错点,根据物料守恒和电荷守恒来分析解答.

练习册系列答案
相关题目
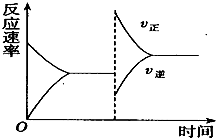 如图是关于反应A2(g)+B2(g)?2C(g)+D(g)△H<0的平衡移动图象,影响平衡移动的原因可能是( )
如图是关于反应A2(g)+B2(g)?2C(g)+D(g)△H<0的平衡移动图象,影响平衡移动的原因可能是( )| A、升高温度,同时加压 |
| B、压强不变,降低温度 |
| C、压强、温度不变,充入一些与之不反应的惰性气体 |
| D、温度、压强不变,充入一些A2(g) |
NA为阿伏加德罗常数,下列叙述错误的是( )
| A、常温常压下,22.4L CH4含有NA个CH4分子 |
| B、18 gH2O中含有的质子数为10NA |
| C、46 g NO2和N2O4混合气体中含有原子总数为3NA |
| D、在18g 18O2中含有NA个氧原子 |
 下图表示的一些物质或概念间的从属关系中正确的是( )
下图表示的一些物质或概念间的从属关系中正确的是( )| X | Y | Z | |
| A | 氧化钙 | 氧化物 | 碱性氧化物 |
| B | 盐 | 化合物 | 电解质 |
| C | 胶体 | 分散系 | 混合体系 |
| D | 置换反应 | 氧化还原反应 | 离子反应 |
| A、A | B、B | C、C | D、D |
下列说法正确的是( )
| A、熔融状态的HgCl2不能导电,HgCl2的稀溶液有弱的导电能力且可作手术刀的消毒液,从不同角度分类HgCl2是一种共价化合物、非电解质、盐、分子晶体 |
| B、单质熔点97.81℃,是热和电的良导体,该晶体最可能是分子晶体 |
| C、SiO2晶体属于原子晶体,1mol的SiO2晶体含有4NA的Si-O键(NA为阿伏伽德罗常数) |
| D、固态金属单质都是金属晶体,金属晶体含有金属键.非金属单质晶体都是分子晶体,分子晶体主要含有共价键,范德华力,有些分子晶体还含有氢键 |
下列反应属于取代反应的是( )
| A、乙炔→乙烯 |
| B、乙醛→乙酸 |
| C、乙醛→乙醇 |
| D、乙醇→溴乙烷 |
下列关于叙述正确的是( )
| A、物质的量是含有一定数目粒子的集合体 |
| B、摩尔质量就是该物质的相对分子质量或相对原子质量 |
| C、单位物质的量的物质所占的体积就是气体摩尔体积 |
| D、40gNaOH溶解在1L水中,形成溶液溶质的物质的量浓度为1mol/L |
在标准状况下,相同体积的H2、O2、N2三种气体,有关叙述正确的是( )
| A、分子数相同 | B、质量相同 |
| C、原子数相同 | D、密度相同 |