题目内容
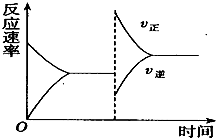 如图是关于反应A2(g)+B2(g)?2C(g)+D(g)△H<0的平衡移动图象,影响平衡移动的原因可能是( )
如图是关于反应A2(g)+B2(g)?2C(g)+D(g)△H<0的平衡移动图象,影响平衡移动的原因可能是( )| A、升高温度,同时加压 |
| B、压强不变,降低温度 |
| C、压强、温度不变,充入一些与之不反应的惰性气体 |
| D、温度、压强不变,充入一些A2(g) |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:A、升高温度,同时加压,正逆反应速率都增大,升高温度,使平衡向逆反应移动,增大压强,使平衡向正反应移动,平衡可能不移动,可能向正反应移动,可能向逆反应移动.
B、降低温度,正逆反应速率都降低,降低温度,使平衡向正反应移动;
C、恒温恒压容器 充入惰气,为保持恒压,压强减小,平衡向正反应移动;
D、增大反应物浓度,正逆反应速率都增大,但正反应速率增大更多,平衡向正反应移动.
B、降低温度,正逆反应速率都降低,降低温度,使平衡向正反应移动;
C、恒温恒压容器 充入惰气,为保持恒压,压强减小,平衡向正反应移动;
D、增大反应物浓度,正逆反应速率都增大,但正反应速率增大更多,平衡向正反应移动.
解答:
解:A、升高温度,同时加压,正逆反应速率都增大,逆反应速率大于正反应速率,逆反应速率大于正反应速率,逆反应速率应在原速率的上方,故A错误;
B、降低温度,正逆反应速率都降低,正反应速率应在原速率的下方,故B错误;
C、压强、温度不变,充入一些与之不反应的惰性气体,体积增大,平衡正向进行,速率减小,故C错误;
D、增大反应物浓度,为保持恒压,瞬间逆反应速率减小,但随反应进行,正逆反应速率都增大,正向进行气体压强增大,所以逆反应速率在原速率的下方,但正反应速率增大更多,平衡向正反应移动,故D正确.
故选:D.
B、降低温度,正逆反应速率都降低,正反应速率应在原速率的下方,故B错误;
C、压强、温度不变,充入一些与之不反应的惰性气体,体积增大,平衡正向进行,速率减小,故C错误;
D、增大反应物浓度,为保持恒压,瞬间逆反应速率减小,但随反应进行,正逆反应速率都增大,正向进行气体压强增大,所以逆反应速率在原速率的下方,但正反应速率增大更多,平衡向正反应移动,故D正确.
故选:D.
点评:本题考查了外界条件对化学反应速率和平衡的影响、平衡移动图象,难度较大,明确温度、压强、浓度变化引起化学反应速率变化是解本题的关键.

练习册系列答案
相关题目
下列物质可用分液漏斗分离的是( )
| A、碘与酒精 | B、硝基苯与水 |
| C、苯与溴苯 | D、苯磺酸与水 |
下面是有关厨房中的常见操作或常见现象,其中不属于氧化还原反应的是( )
| A、烧菜用过的铁锅,经放置常出现红棕色锈斑 |
| B、用醋酸除去水壶或锅中的水垢[主要成分CaCO3] |
| C、用煤气灶燃烧沼气[主要成分甲烷(CH4)]为炒菜提供热量 |
| D、牛奶久置变质腐败 |
进入人体的O2有2%转化为“活性氧”,它能加速人的衰老,被称为“生命杀手”,服用亚硒酸钠(Na2SeO3)能消除人体内的“活性氧”.下列说法正确的是( )
| A、Na2SeO3在反应中做还原剂 |
| B、Na2SeO3在反应中做氧化剂 |
| C、亚硒酸钠中硒的化合价为+4价 |
| D、“活性氧”在反应中做催化剂 |
下列各组混合物的分离或提纯方法正确的是( )
| A、提纯NaCl和KNO3的混合物中的KNO3:加热蒸发、冷却结晶,过滤 |
| B、除去CO2中混有的少量CO:混合气体依次通过NaOH溶液和浓硫酸 |
| C、除去盐酸溶液中混有的少量CaCl2:加入过量CaCO3粉末,过滤 |
| D、除去NaCl溶液中混有的少量I2:向混合溶液中加入适量CCl4,充分振荡,分液 |
下列物质的水溶液能导电,但属于非电解质的是( )
| A、Na2S |
| B、HCl |
| C、NaHCO3 |
| D、NH3 |
下列各物质的分类、名称(或俗名)、化学式都正确的是( )
| A、碱、纯碱、Na2CO3 |
| B、单质、氯水、Cl2 |
| C、酸、硫酸、H2S |
| D、酸性氧化物、干冰、CO2 |
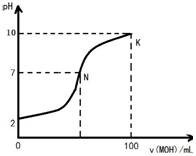 常温下,向100mL 0.01mol?L-1盐酸中逐滴加入0.02mol?L-1 MOH溶液,如图所示,曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计).下列说法中不正确的是( )
常温下,向100mL 0.01mol?L-1盐酸中逐滴加入0.02mol?L-1 MOH溶液,如图所示,曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计).下列说法中不正确的是( )| A、MOH是弱碱 | ||
| B、N点c(Cl-)=c(M+) | ||
C、随着MOH溶液的滴加,比值
| ||
| D、K点对应的溶液c(MOH)+c(OH-)-c(H+)=0.001mol?L-1 |