题目内容
NA为阿伏加德罗常数,下列叙述错误的是( )
| A、常温常压下,22.4L CH4含有NA个CH4分子 |
| B、18 gH2O中含有的质子数为10NA |
| C、46 g NO2和N2O4混合气体中含有原子总数为3NA |
| D、在18g 18O2中含有NA个氧原子 |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、气体摩尔体积的条件应用分析,标准状况22,4L气体为1mol;
B、依据n=
计算物质的量结合分子式计算质子数;
C、NO2和N2O4混合气体最简式相同为NO2,只需要计算46 g NO2中原子数;
D、依据n=
计算物质的量结合分子式计算原子数.
B、依据n=
| m |
| M |
C、NO2和N2O4混合气体最简式相同为NO2,只需要计算46 g NO2中原子数;
D、依据n=
| m |
| M |
解答:
解:A、气体摩尔体积的条件应用分析,标准状况22,4L气体为1mol,常温常压下,22.4L CH4物质的量不是1mol,不一定含有NA个CH4分子,故A错误;
B、依据n=
计算物质的量=
=1mol,结合分子式计算质子数为10NA,故B正确;
C、NO2和N2O4混合气体最简式相同为NO2,只需要计算46 g NO2中原子数=
×3×NA=3NA,故C正确;
D、依据n=
计算物质的量=
=0.5mol,结合分子式计算原子数=0.5mol×2×NA=NA个,故D正确;
故选A.
B、依据n=
| m |
| M |
| 18g |
| 18g/mol |
C、NO2和N2O4混合气体最简式相同为NO2,只需要计算46 g NO2中原子数=
| 46g |
| 46g/mol |
D、依据n=
| m |
| M |
| 18g |
| 36g/mol |
故选A.
点评:本题考查了阿伏伽德罗常数的分析应用,主要是物质的量和质量、气体体积、微粒数的计算应用,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
下列物质可用分液漏斗分离的是( )
| A、碘与酒精 | B、硝基苯与水 |
| C、苯与溴苯 | D、苯磺酸与水 |
下列物质的水溶液能导电,但属于非电解质的是( )
| A、Na2S |
| B、HCl |
| C、NaHCO3 |
| D、NH3 |
下列各物质的分类、名称(或俗名)、化学式都正确的是( )
| A、碱、纯碱、Na2CO3 |
| B、单质、氯水、Cl2 |
| C、酸、硫酸、H2S |
| D、酸性氧化物、干冰、CO2 |
下列说法中正确的是( )
| A、1L 水中溶解了58.5g NaCl,该溶液的物质的量浓度为1mol/L |
| B、从1L 2mol/L的H2SO4溶液中取出0.5L,该溶液的浓度为1mol/L |
| C、配制500mL 0.2mol/L的CuSO4溶液,需25g胆矾 |
| D、中和100mL 1mol/L的H2SO4溶液,需NaOH 4g |
在某澄清、透明的浅黄色溶液中,可能含有下列八种离子:H+、NH
、Fe3+、Ba2+、Al3+、SO
、CO32-、I-,在检验方案设计时初步分析其溶液中最多可含离子(不包括OH-)有( )
+ 4 |
2- 4 |
| A、4种 | B、5种 | C、6种 | D、7种 |
下列说法错误的是( )
| A、需要加热才能发生的反应不一定是吸热反应 |
| B、放热反应在常温下一定很容易发生 |
| C、反应是放热还是吸热取决于反应物和生成物所具有的总能量的相对大小 |
| D、吸热的反应在常温下也可能发生 |
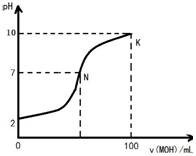 常温下,向100mL 0.01mol?L-1盐酸中逐滴加入0.02mol?L-1 MOH溶液,如图所示,曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计).下列说法中不正确的是( )
常温下,向100mL 0.01mol?L-1盐酸中逐滴加入0.02mol?L-1 MOH溶液,如图所示,曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计).下列说法中不正确的是( )| A、MOH是弱碱 | ||
| B、N点c(Cl-)=c(M+) | ||
C、随着MOH溶液的滴加,比值
| ||
| D、K点对应的溶液c(MOH)+c(OH-)-c(H+)=0.001mol?L-1 |
用价层电子对互斥理论(VSEPR)可以预测许多分子或离子的空间构型,有时也能用来推测键角大小,下列判断正确的是( )
| A、SO2、CS2、HI都是直线形的分子 |
| B、BF3键角为120°,SnBr2键角大于120° |
| C、COCl2、BF3、SO3都是平面三角形的分子 |
| D、PCl3、NH3、PCl5都是三角锥形的分子 |