题目内容
4.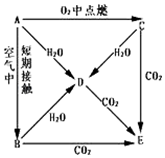 A、B、C、D、E五种物质焰色反应均为黄色,它们按图所示关系相互转化.
A、B、C、D、E五种物质焰色反应均为黄色,它们按图所示关系相互转化.(1)这五种物质中,A:Na、C:Na2O2.
(2)将CO2通入E的饱和溶液中,该反应的离子方程式为CO2+H2O+2Na++CO32-=2NaHCO3↓.
(3)写出A→D、C→D、C→E反应的化学方程式
A→D:2Na+H2O=2NaOH+H2↑
C→D:2Na2O2+2H2O=4NaOH+O2↑
C→E:2Na2O2+2CO2=2Na2CO3+O2.
分析 A在氧气中燃烧生成C,A在空气中短期接触生成B,A与水反应生成D,且A、B、C都能和水反应生成D,B、C都是氧化物,都和水反应生成D,D只能为碱A、B、C、D、E五种物质的焰色反应均为黄色说明含有钠元素,故A为Na,C为Na2O2,D为NaOH,E是Na2CO3,Na在空气中短期接触生成B,B为Na2O,Na2O与CO2反应生成Na2CO3,与水反应生成NaOH,符合转化关系,以此解答该题.
解答 解:(1)由以上分析可知A为Na,C为Na2O2,故答案为:Na;Na2O2;
(2)E是Na2CO3,将CO2通入E的饱和溶液中,生成碳酸氢钠沉淀,反应的离子方程式为CO2+H2O+2Na++CO32-=2NaHCO3↓,
故答案为:CO2+H2O+2Na++CO32-=2NaHCO3↓;
(3)A→D的反应是钠和水反应生成氢氧化钠和氢气,反应的化学方程式为:2Na+2H2O=2NaOH+H2↑,C→D为过氧化钠和水的反应,化学方程式为2Na2O2+2H2O=4NaOH+O2↑,过氧化钠和二氧化碳反应生成碳酸钠和氧气,方程式为2Na2O2+2CO2=2Na2CO3+O2,
故答案为:2Na+H2O=2NaOH+H2↑;2Na2O2+2H2O=4NaOH+O2↑;2Na2O2+2CO2=2Na2CO3+O2.
点评 本题以无机框图题的形式考查Na元素单质及其化合物之间的相互转化关系、化学用语的书写等,为高考常见题型和高频考点,比较基础,结合转化关系判断D为碱是关键,推断金属A为Na,然后进行验证,题目难度不大.

练习册系列答案
相关题目
15.现有盐酸、NaCl溶液、NaOH溶液和新制氯水,可用来区别它们的试剂是( )
| A. | 酚酞试液 | B. | 紫色石蕊试液 | C. | AgNO3 溶液 | D. | NaHCO3溶液 |
12.某无色透明溶液中,能大量共存的离子组是( )
| A. | Na、K+、SO42-、HCO3- | B. | Cu2+、K+、SO42-、NO3- | ||
| C. | NH4+、K+、Cl-、OH- | D. | Fe3+、K+、SCN-、Cl- |
19.通常人们把拆开1mol某化学键所吸收的能量看成该化学键的键能.现给出化学键的键能(见表):
请计算H2(g)+Br2(g)═2HBr(g)的反应热( )
| 化学键 | H-H | Br-Br | H-Br |
| 键能/(kJ•mol-1) | 436 | 193 | 366 |
| A. | +103 kJ•mol-1 | B. | +679 kJ•mol-1 | C. | -103 kJ•mol-1 | D. | +183 kJ•mol-1 |
13.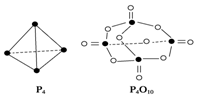 白磷与氧气可发生如下反应:P4+5O2═P4O10已知断裂下列化学键需要吸收的能量分别 为P-O:a kJ•mol-1、P-P:b kJ•mol-1、P═O:c kJ•mol-1 O═O:d kJ•mol-1.根据如图所示的分子结构和有关数据估算该反应的△H,其中正确的是( )
白磷与氧气可发生如下反应:P4+5O2═P4O10已知断裂下列化学键需要吸收的能量分别 为P-O:a kJ•mol-1、P-P:b kJ•mol-1、P═O:c kJ•mol-1 O═O:d kJ•mol-1.根据如图所示的分子结构和有关数据估算该反应的△H,其中正确的是( )
 白磷与氧气可发生如下反应:P4+5O2═P4O10已知断裂下列化学键需要吸收的能量分别 为P-O:a kJ•mol-1、P-P:b kJ•mol-1、P═O:c kJ•mol-1 O═O:d kJ•mol-1.根据如图所示的分子结构和有关数据估算该反应的△H,其中正确的是( )
白磷与氧气可发生如下反应:P4+5O2═P4O10已知断裂下列化学键需要吸收的能量分别 为P-O:a kJ•mol-1、P-P:b kJ•mol-1、P═O:c kJ•mol-1 O═O:d kJ•mol-1.根据如图所示的分子结构和有关数据估算该反应的△H,其中正确的是( )| A. | (6b+5d-4c-12a) kJ•mol-1 | B. | (4b+5d-4c-12a) kJ•mol-1 | ||
| C. | (4c+12a-4b-5d) kJ•mol-1 | D. | (4c+12a-6b-5d) kJ•mol-1 |
 Cl2(g)===AgCl(s) ΔH=-127 kJ·mol-1
Cl2(g)===AgCl(s) ΔH=-127 kJ·mol-1