题目内容
11.到目前为止,由化学能转变为热能或电能仍然是人类使用的最主要能源.(1)化学反应中放出的热能(焓变,△H)与反应物和生成物在反应过程中断键和形成新键过程中吸收和放出能量的大小有关.
已知:H2(g)+Cl2(g)═2HCl(g)△H=-185kJ/mol,断裂1mol H-H键吸收的能量为436kJ,断裂1mol Cl-Cl键吸收的能量为247kJ,则形成1mol H-Cl键放出的能量为434KJ/mol.
(2)燃料燃烧将其所含的化学能转变为我们所需要的热能.已知:
①CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890.3kJ•mol-1
②C(s,石墨)+O2(g)═CO2(g)△H=-393.5kJ•mol-1
③2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ•mol-1
标准状况下22.4L氢气和甲烷的混合气体在足量的氧气中充分燃烧反应放出588.05kJ的热量,原混合气体中氢气的质量是1g.根据以上三个热化学方程式,计算C(s,石墨)+2H2(g)═CH4(g)的反应热△H为-74.8KJ/mol.
分析 (1)反应热=反应物总键能-生成物总键能,据此计算;
(2)令氢气和甲烷的物质的量分别为xmol、ymol,根据二者体积与燃烧放出的热量列方程计算x、y的值,再根据m=nM计算氢气的质量;
根据盖斯定律构造目标热化学方程式,据此计算解答.
解答 解:(1)断裂1mol H-H键吸收的能量为436kJ,断裂1mol Cl-Cl键吸收的能量为247kJ,由反应化学方程式H2(g)+Cl2(g)═2HCl(g)△H=-185kJ/mol,可知436kJ/mol+247kJ/mol-2E(H-Cl)=-185kJ/mol,解得E(H-Cl)=434KJ/mol,
故答案为:434KJ/mol;
(2)令氢气和甲烷的物质的量分别为xmol、ymol,根据二者体积与燃烧放出的热量,则:
$\left\{\begin{array}{l}{x+y=\frac{22.4}{22.4}}\\{\frac{571.6}{2}x+890.3y=588.05}\end{array}\right.$,解得x=0.5mol,y=0.5mol,
故氢气的质量为0.5mol×2g/mol=1g,
已知:①CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890.3 KJ•mol-1
②C(石墨)+O2(g)═CO2(g)△H=-393.5KJ•mol-1
③2H2(g)+O2(g)═2H2O(l)△H=-571.6 KJ•mol-1
根据盖斯定律,②+③-①得C(石墨)+2H2(g)=CH4(g),故△H=(-393.5KJ/mol)+(-571.6KJ/mol)-(-890.3KJ/mol)=-74.8KJ/mol,
故答案为:1g;-74.8KJ/mol.
点评 本题考查反应热的有关计算,难度中等,注意掌握根据盖斯定律、热化学方程式、燃烧热等进行的计算.

| 选项 | X | Y | Z | M |
| A | Fe(s) | FeCl2 | FeCl3 | Cl2 |
| B | NaOH(aq) | Na2CO3 | NaHCO3 | CO2 |
| C | NH3(g) | NO | NO2 | O2 |
| D | NaOH | NOAlO2 | Al(OH)3 | AlCl3 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 25℃,pH=13的NaOH溶液中含有OH-的数目为0.1NA | |
| B. | 常温下,1 L 0.1 mol•L-1的NH4NO3溶液中氮原子数为0.2NA | |
| C. | 10 L pH=1的硫酸溶液中含有的H+为2NA | |
| D. | 欲配制1.00 L 1.00 mol•L-1的NaCl溶液,可将58.5 g NaCl溶于1.00 L水中 |
| A. | 氢氟酸应保存在塑料盖的玻璃瓶中 | |
| B. | 浓盐酸一定要存放在棕色瓶中,可防止挥发 | |
| C. | 液溴应盛放在橡胶塞的棕色瓶中 | |
| D. | 固态碘应放在广口瓶中 |
| 酸 | 电离常数K |
| HX | 9×10-7 |
| HY | 9×10-6 |
| HZ | 1×10-2 |
| A. | 三种酸的强弱关系:HX>HY>HZ | |
| B. | 反应HZ+Y -=HY+Z -能够发生 | |
| C. | 相同温度下,0.1mol/L的NaX、NaY、NaZ溶液,NaZ溶液pH最大 | |
| D. | 相同温度下,1mol/L HX溶液的电离常数大于0.1mol/L HX |
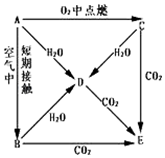 A、B、C、D、E五种物质焰色反应均为黄色,它们按图所示关系相互转化.
A、B、C、D、E五种物质焰色反应均为黄色,它们按图所示关系相互转化. .(不考虑空间构型)
.(不考虑空间构型)