题目内容
7.下列离子方程式书写正确的是( )| A. | 向次氯酸钙溶液通过量CO2:Ca2++2ClO-+H2O+CO2═CaCO3↓+2HClO | |
| B. | 向Ca(HCO3)2溶液中加入过量的NaOH溶液:Ca2++HCO3-+OH-═CaCO3↓+CO32-+H2O | |
| C. | 酸性溶液中KIO3与KI反应生成I2:IO3-+5I-+6H+=3I2+3H2O | |
| D. | 氢氧化钡溶液中加入硫酸:Ba2++OH-+H++SO42-═BaSO4+H2O |
分析 A.反应生成碳酸氢钙、HClO;
B.反应生成碳酸钙、碳酸钠和水;
C.发生氧化还原反应,遵循电子、电荷守恒;
D.不符合离子的配比.
解答 解:A.向次氯酸钙溶液通过量CO2的离子反应为ClO-+H2O+CO2═HCO3-+HClO,故A错误;
B.向Ca(HCO3)2溶液中加入过量的NaOH溶液的离子反应为Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+H2O,故B错误;
C.酸性溶液中KIO3与KI反应生成I2的离子反应为IO3-+5I-+6H+=3I2+3H2O,故C正确;
D.氢氧化钡溶液中加入硫酸的离子反应为Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O,故D错误;
故选C.
点评 本题考查离子反应方程式的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,注意与量有关的离子反应及离子反应中保留化学式的物质,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.下列离子方程式正确的是( )
| A. | 氯碱工业中电解饱和食盐水:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$H2↑+Cl2↑+2OH- | |
| B. | 氯化铁溶液腐蚀铜板:Fe3++Cu=Fe2++Cu2+ | |
| C. | 氢氧化钠溶液吸收少量二氧化硫SO2+OH-=HSO3- | |
| D. | 稀硫酸中加氢氧化钡溶液至中性:Ba2++H++OH-+SO42-=BaSO4↓+H2O |
18.下列各离子组中,能在水溶液中大量共存,当滴加稀硫酸后则不能大量共存的是( )
| A. | Na+、Mg2+、Cl-、I- | B. | Fe2+、Ba2+、S2-、Cl- | ||
| C. | Na+、Al3+、Cl-、HCO3- | D. | K+、Fe2+、Cl-、NO3- |
19.下列离子方程式中书写正确的是( )
| A. | 向FeCl2溶液中通入Cl2反应生成FeCl3溶液:Fe2++Cl2═Fe3++2Cl- | |
| B. | CO2通入过量的NaOH溶液:CO2+OH-═HCO3- | |
| C. | 大理石溶于硝酸:CaCO3+2H+═Ca2++CO2↑+H2O | |
| D. | 碳酸钡和稀硫酸:BaCO3+2H+═Ba2++CO2↑+H2O |
17.下列装置或操作不正确的是( )
| A. | 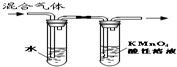 装置可用于检验溴乙烷消去反应的产物 | |
| B. | 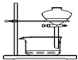 装置可用于放出碘的四氯化碳溶液 | |
| C. | 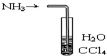 装置可用于吸收NH3防止倒吸 | |
| D. | 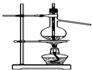 装置可用于实验室制备蒸馏水 |