题目内容
13.关注饮用水,保证人民的生活质量.回答下列两个问题:(1)饮用水中的NO3-对人类健康会产生危害,为了降低饮用水中NO3-的浓度,可以在碱性条件下用铝粉将NO3-还原为N2,其化学方程式为:
10Al+6NaNO3+4NaOH═10NaAlO2+3N2↑+2H2O.请回答下列问题:
①上述反应中,Al元素的化合价升高,则该元素的原子失去(填“得到”或“失去”)电子
②用“单线桥法”表示反应中电子转移的方向和数目:
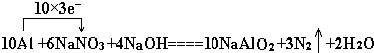
(2)洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一.漂白粉是常用的消毒剂.
①工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学反应方程式为2Ca(OH)2+2Cl2═CaCl2+Ca(ClO)2+2H2O.
②漂白粉的有效成分是(填化学式)Ca(ClO)2.
③漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,离子方程式为Ca2++2ClO-+CO2+H2O═CaCO3↓+2HClO.
分析 (1)10Al+6NaNO3+4NaOH═10NaAlO2+3N2↑+2H2O中,Al元素的化合价升高,N元素的化合价降低,该反应中转移30e-;
(2)①氯气通入石灰乳[Ca(OH)2],反应生成氯化钙、次氯酸钙、水;
②漂白粉的有效成分为次氯酸钙;
③漂白粉溶于水后,与CO2、水反应生成碳酸钙和次氯酸.
解答 解:(1)①Al元素的化合价由0升高为+3价,失去电子,故答案为:Al;失去;
②10Al+6NaNO3+4NaOH═10NaAlO2+3N2↑+2H2O中,Al元素的化合价升高,N元素的化合价降低,该反应中转移30e-,用“单线桥法”表示反应中电子转移的方向和数目为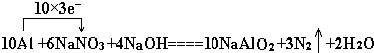 ,
,
故答案为: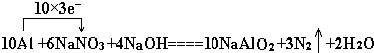 ;
;
(2)①氯气通入石灰乳[Ca(OH)2],反应生成氯化钙、次氯酸钙、水,反应为2Ca(OH)2+2Cl2═CaCl2+Ca(ClO)2+2H2O,
故答案为:2Ca(OH)2+2Cl2═CaCl2+Ca(ClO)2+2H2O;
②漂白粉的有效成分为Ca(ClO)2,故答案为:Ca(ClO)2;
③漂白粉溶于水后,与CO2、水反应生成碳酸钙和次氯酸,离子反应为Ca2++2ClO-+CO2+H2O═CaCO3↓+2HClO,故答案为:Ca2++2ClO-+CO2+H2O═CaCO3↓+2HClO.
点评 本题考查氧化还原反应,为高频考点,把握发生的反应及反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
3.硅是重要的半导体材料,构成了现代电子工业的基础.请回答下列问题:
(1)基态Si原子中,电子占据的最高能层符号为M,该能层具有的原子轨道数为9、电子数为4.
(2)硅主要以硅酸盐、二氧化硅等化合物的形式存在于地壳中.
(3)单质硅存在与金刚石结构类似的晶体,其中原子与原子之间以共价键相结合,其晶胞中共有8个原子,其中在面心位置贡献3个原子.
(4)单质硅可通过甲硅烷(SiH4)分解反应来制备.工业上采用Mg2Si和NH4Cl在液氨介质中反应制得SiH4,该反应的化学方程式为Mg2Si+4NH4Cl=SiH4+4NH3+2MgCl2.
(5)碳和硅的有关化学键键能如下所示,简要分析和解释下列有关事实:
①硅与碳同族,也有系列氢化物,但硅烷在种类和数量上都远不如烷烃多,原因是C-C键和C-H键较强,所形成的烷烃稳定.而硅烷中Si-Si键和Si-H键的键能较低,易断裂,导致长链硅烷难以生成.
②SiH4的稳定性小于CH4,更易生成氧化物,原因是C-H键的键能大于C-O键,C-H键比C-O键稳定.而Si-H键的键能却远小于Si-O键,所以Si-H键不稳定而倾向于形成稳定性更强的Si-O键.
(6)在硅酸盐中,SiO44-四面体;如图(a)通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式.图(b)为一种无限长单链结构的多硅酸根,其中Si原子的杂化形式为sp3,Si与O的原子数之比为1:3,化学式为SiO32-.

(1)基态Si原子中,电子占据的最高能层符号为M,该能层具有的原子轨道数为9、电子数为4.
(2)硅主要以硅酸盐、二氧化硅等化合物的形式存在于地壳中.
(3)单质硅存在与金刚石结构类似的晶体,其中原子与原子之间以共价键相结合,其晶胞中共有8个原子,其中在面心位置贡献3个原子.
(4)单质硅可通过甲硅烷(SiH4)分解反应来制备.工业上采用Mg2Si和NH4Cl在液氨介质中反应制得SiH4,该反应的化学方程式为Mg2Si+4NH4Cl=SiH4+4NH3+2MgCl2.
(5)碳和硅的有关化学键键能如下所示,简要分析和解释下列有关事实:
| 化学键 | C-C | C-H | C-O | Si-Si | Si-H | Si-O |
| 键能/(kJ•mol-1) | 356 | 413 | 336 | 226 | 318 | 452 |
②SiH4的稳定性小于CH4,更易生成氧化物,原因是C-H键的键能大于C-O键,C-H键比C-O键稳定.而Si-H键的键能却远小于Si-O键,所以Si-H键不稳定而倾向于形成稳定性更强的Si-O键.
(6)在硅酸盐中,SiO44-四面体;如图(a)通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式.图(b)为一种无限长单链结构的多硅酸根,其中Si原子的杂化形式为sp3,Si与O的原子数之比为1:3,化学式为SiO32-.

1.下列说法正确的是( )
| A. | 过氧化钠、纯碱分别属于碱性氧化物、碱 | |
| B. | NO、NO2 都是大气污染物,在空气中都能稳定存在 | |
| C. | SiO2能与NaOH溶液、HF溶液反应,所以SiO2是两性氧化物 | |
| D. | 检验某浅绿色溶液中含有Fe2+:取该溶液少许,向其中加入KSCN溶液,不变红色,再向其中滴加氯水,溶液变为红色 |
8.化学与社会、生产、生活密切相关.下列说法正确的是( )
| A. | 用激光笔分别照射盛有牛奶、食盐水的玻璃杯,都有光亮的通路 | |
| B. | 神舟10号飞船所用太阳能电池板可将光能转换为电能,转换材料是二氧化硅 | |
| C. | 氯气溶于水生成次氯酸有强氧化性,可以起到除去水中杂质和杀菌消毒作用 | |
| D. | 可以用物理方法或化学方法从海水中提取所需物质 |
18.下列离子方程式正确的是( )
| A. | 磁性氧化铁溶于稀硝酸:3Fe2++4H++NO3-═3Fe3++NO↑+3H2O | |
| B. | 向NaAlO2溶液中通入过量CO2制Al(OH)3:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3- | |
| C. | 用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O | |
| D. | 在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO-+2Fe(OH)3═2FeO42-+3Cl-+H2O+4H+ |
5.某有机物的结构简式为CH3-CH=CH-COOH.现有①铁;②溴的四氯化碳溶液;③碳酸氢钠溶液;④丙醇;⑤酸性高锰酸钾溶液,判断在一定条件下,能与该有机物反应的物质是( )
| A. | 仅②④⑤ | B. | 仅①③④ | C. | 仅①②③④ | D. | ①②③④⑤ |
2.下列事实中,使用牺牲阳极的阴极保护法进行金属防腐的是( )
| A. | 地下钢管连接镁块 | B. | 金属护栏表面涂漆 | ||
| C. | 汽车底盘喷涂高分子膜 | D. | 水中的钢闸门连接电源的负极 |
 在实验室里制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫,有人设计了下列实验图以确认上述混合气体中有CH2=CH2和SO2.
在实验室里制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫,有人设计了下列实验图以确认上述混合气体中有CH2=CH2和SO2.
