题目内容
1. 实验室要用Na2CO3•10H2O晶体配制500mLO.1mol•L-1Na2CO3溶液,回答下列问题:
实验室要用Na2CO3•10H2O晶体配制500mLO.1mol•L-1Na2CO3溶液,回答下列问题:(1)应该用托盘天平称取Na2CO3•10H2O14.3g.
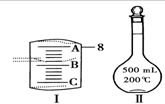
(2)右翻I表示10mL量筒中液面的位置,A与B,B与C刻度间相差1mL,如果刻度A为8,量筒中液体的体积是7.2mL.
分析 (1)依据m=CVM计算需要溶质Na2CO3•10H2O晶体的质量;
(2)依据量筒小数在下,大数在上,精确度为0.1mL解答.
解答 解:(1)用Na2CO3•10H2O晶体配制500mLO.1mol•L-1Na2CO3溶液,需要溶质Na2CO3•10H2O晶体的质量=0.1mol/L×0.5L×286g/mol=14.3g;
故答案为:14.3;
(2)从图中可知,A为8mL,A-B之间有5个空格,每一空格代表0.2mL,所以量筒中液体的体积为7.2mL;
故答案为:7.2.
点评 本题考查了有关物质的量的计算、量筒读数,题目难度不大,注意量筒的构造及精确度.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
11.图是一套检验气体性质的实脸装置.向装里中缓慢通入气体X.若关闭活塞,溉清石灰水变浑浊;若打开活塞,则品红溶液褪色,据此判断气体X 和洗气瓶内的溶液Y可能是( )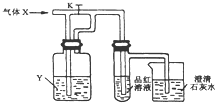

| A. | X是SO2,Y是饱和NaHCO3 溶液 | B. | X是H2S,Y是浓H2SO4 | ||
| C. | X是CO2,Y是Na2SO3 溶液 | D. | X是Cl2,Y是Na2CO3溶液 |
12.下列离子在水溶液中能大量共存的是( )
| A. | Cl-、K+、HCO3-、Ca2+ | B. | OH-、NH4+、Mg2+、HCO3- | ||
| C. | SO32-、H+、Cl-、NO3- | D. | Na+、SiO32-、H+、Cl- |
9.下列各组离子在指定条件下,一定不能大量共存的是( )
| A. | 加入Al能放出H2的溶液中:K+、Na+、CO32-、NO3- | |
| B. | 滴入甲基橙变黄的溶液中:Cu2+、Al3+、SO42-、NO3- | |
| C. | 能使碘化钾淀粉试纸变蓝的溶液中:Na+、NH4+、S2-、Br- | |
| D. | 水电离出的c(H+)=1×10-12 mol•L-1的溶液中:Na+、Mg2+、Cl-、SO42- |
16.下列说法正确的是( )
| A. | 所有需要加热的反应都是吸热反应 | |
| B. | 所有金属元素形成的化合物都是离子化合物 | |
| C. | 所有主族元素的族序数等于其原子最外层上的电子数 | |
| D. | 所有共价化合物分子中每个原子最外层都达到稀有气体的稳定结构 |
6.下列物质中,既能跟盐酸反应,又能跟NaOH溶液反应的是( )
| A. | NaHCO3 | B. | Fe2O3 | C. | Al2O3 | D. | SiO2 |
11.下列说法正确的是( )
| A. | 需要加热发生的反应一定是吸热反应 | |
| B. | 任何放热反应在常温下一定能发生 | |
| C. | 温度压强一定时,放热的、熵增加反应能自发进行 | |
| D. | 吸热反应一定是反应物总能量大于生成物的总能量 |
 .
.