题目内容
11.图是一套检验气体性质的实脸装置.向装里中缓慢通入气体X.若关闭活塞,溉清石灰水变浑浊;若打开活塞,则品红溶液褪色,据此判断气体X 和洗气瓶内的溶液Y可能是( )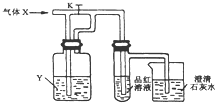
| A. | X是SO2,Y是饱和NaHCO3 溶液 | B. | X是H2S,Y是浓H2SO4 | ||
| C. | X是CO2,Y是Na2SO3 溶液 | D. | X是Cl2,Y是Na2CO3溶液 |
分析 二氧化硫具有漂白性,干燥氯气不具有漂白性,氯气与水反应生成的次氯酸具有漂白性,能够使澄清的石灰水变浑浊的气体可能为二氧化硫或者二氧化碳,据此分析解答.
解答 解:A.二氧化硫具有漂白性,能够使品红褪色,若关闭活塞,SO2与NaHCO3溶液反应生成CO2气体,品红溶液无变化,澄清石灰水变浑浊;若打开活塞,SO2使品红褪色,故A正确;
B.硫化氢不具有漂白性,所以打开活塞,品红溶液不褪色,故B错误;
C.二氧化碳不具有漂白性,且与亚硫酸钠不反应,所以无论打开或者关闭活塞,品红溶液都不褪色,故C错误;
D.若打开活塞,氯气通入品红溶液,能够使其褪色,若关闭活塞,氯气通入碳酸钠溶液发生反应,氯气被吸收,生成二氧化碳,所以品红溶液无变化而澄清的石灰水变浑浊,故D正确;
故选:AD.
点评 本题考查了常见气体的检验,熟悉氯气、二氧化硫、二氧化碳的性质是解题关键,注意氯气不具有漂白性,具有漂白性的是次氯酸,题目难度中等.

练习册系列答案
相关题目
1.(1)已知在常温常压下:
①2CH3OH(I)+3O2(g)═2CO2(g)+4H2O(g)△H=-1275.6kJ/mol
②2CO(g)+O2(g)═2CO2(g)△H=-566.0kJ/mol
③H2O(g)═H2O(I)△H=-44.0kJ/mol
请写出1mol甲醇不完全燃烧生成1mol一氧化碳和液态水的热化学方程式:CH3OH(l)+O2(g)=CO(g)+2H2O(l)△H=-442.8kJ/mol.
(2)甲醇对水质会造成一定的污染,有一种电化学法可消除这种污染,其原理是:通电后将Co2+氧化成Co3+,然后以Co3+做氧化剂把水中的甲醇氧化成CO2而净化.实验室用如图1装置模拟上述过程:

①写出阳极电极反应式Co2+-e-=Co3+;
②除去甲醇的离子反应为:6Co3++CH3OH+H2O═CO2↑+6Co2++6H+.该过程中被氧化的元素是碳,当产生标准状况下2.24LCO2时,共转移电子0.6mol.
(3)测定稀硫酸和稀氢氧化钠中和热的实验装置如图2所示.0.50mol/LNaOH溶液50mL和0.50mol/L硫酸溶液30mL进行实验,实验数据如表所示.
①请写下表中的空白.
②近似认为0.50mol/LNaOH溶液和0.50mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/(g•℃),则中和热△H=-53.5kJ/mol(取小数点后一位).
③上述实验数值与57.3kJ/mol有偏差,产生偏差的原因可能是acd.
a.实验装置保湿或隔热效果差 b.用量筒量取NaOH溶液的体积时俯视读数
c.用环形铜丝搅拌棒搅拌溶液 d用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度.
①2CH3OH(I)+3O2(g)═2CO2(g)+4H2O(g)△H=-1275.6kJ/mol
②2CO(g)+O2(g)═2CO2(g)△H=-566.0kJ/mol
③H2O(g)═H2O(I)△H=-44.0kJ/mol
请写出1mol甲醇不完全燃烧生成1mol一氧化碳和液态水的热化学方程式:CH3OH(l)+O2(g)=CO(g)+2H2O(l)△H=-442.8kJ/mol.
(2)甲醇对水质会造成一定的污染,有一种电化学法可消除这种污染,其原理是:通电后将Co2+氧化成Co3+,然后以Co3+做氧化剂把水中的甲醇氧化成CO2而净化.实验室用如图1装置模拟上述过程:

①写出阳极电极反应式Co2+-e-=Co3+;
②除去甲醇的离子反应为:6Co3++CH3OH+H2O═CO2↑+6Co2++6H+.该过程中被氧化的元素是碳,当产生标准状况下2.24LCO2时,共转移电子0.6mol.
(3)测定稀硫酸和稀氢氧化钠中和热的实验装置如图2所示.0.50mol/LNaOH溶液50mL和0.50mol/L硫酸溶液30mL进行实验,实验数据如表所示.
①请写下表中的空白.
| 温度 实验次数 | 起始温度t1/℃ | 终止温度t℃/℃ | 温度差平均值(t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | 4.0 |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
③上述实验数值与57.3kJ/mol有偏差,产生偏差的原因可能是acd.
a.实验装置保湿或隔热效果差 b.用量筒量取NaOH溶液的体积时俯视读数
c.用环形铜丝搅拌棒搅拌溶液 d用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度.
2.某科研小组探究工业废Cu粉(杂质可能含有SiO2、Al2O3、Fe2O3中的一种或几种)的组成并制备少量CuSO4•5H2O,实现废物综合利用.他们进行了两组实验,过程如下:
Ⅰ: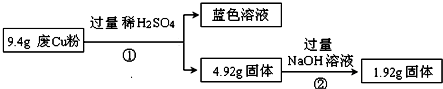
Ⅱ:
(1)废Cu粉中含有的杂质是SiO2、Fe2O3.
(2)分别写出过程①③中发生反应的离子方程式:
①Fe2O3+6H+═2Fe3++3H2O、Al2O3+6H+═2Al3++3H2O、Cu+2Fe3+═2Fe2++Cu2+;③SiO2+2OH-═SiO32-+H2O、Al2O3+2OH-=2AlO2-+H2O.
(3)综合过程Ⅰ、II,计算工业废Cu粉中各成分的质量之比是m(Fe2O3):m(Cu):m(SiO2)=16:16:15(可不必化简).(4)已知25℃时:
从Ⅱ中所得蓝色溶液中分离提纯得到CuSO4•5H2O晶体,需要经过下列步骤:
a、向蓝色溶液中加入一定量的H2O2 溶液;
b、调节溶液的pH为4.0≤pH<5.4之间;
c、然后过滤、结晶,再过滤,可得CuSO4•5H2O.
下列关于实验操作的叙述中,正确的是ACD(填字母).
A.H2O2是绿色氧化剂,在氧化过程中不引进杂质、不产生污染
B.将Fe2+氧化为Fe3+的主要原因是Fe(OH)2沉淀比Fe(OH)3沉淀较难过滤
C.上述步骤c中第一次过滤是为了得到滤液,第二次过滤是为了得到固体
D.在pH>4的溶液中Fe3+一定不能大量存在.
Ⅰ:

Ⅱ:

(1)废Cu粉中含有的杂质是SiO2、Fe2O3.
(2)分别写出过程①③中发生反应的离子方程式:
①Fe2O3+6H+═2Fe3++3H2O、Al2O3+6H+═2Al3++3H2O、Cu+2Fe3+═2Fe2++Cu2+;③SiO2+2OH-═SiO32-+H2O、Al2O3+2OH-=2AlO2-+H2O.
(3)综合过程Ⅰ、II,计算工业废Cu粉中各成分的质量之比是m(Fe2O3):m(Cu):m(SiO2)=16:16:15(可不必化简).(4)已知25℃时:
| 电解质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀时的pH | 5.4 | 6.5 | 3.5 |
| 完全沉淀时的pH | 6.4 | 9.6 | 4.0 |
a、向蓝色溶液中加入一定量的H2O2 溶液;
b、调节溶液的pH为4.0≤pH<5.4之间;
c、然后过滤、结晶,再过滤,可得CuSO4•5H2O.
下列关于实验操作的叙述中,正确的是ACD(填字母).
A.H2O2是绿色氧化剂,在氧化过程中不引进杂质、不产生污染
B.将Fe2+氧化为Fe3+的主要原因是Fe(OH)2沉淀比Fe(OH)3沉淀较难过滤
C.上述步骤c中第一次过滤是为了得到滤液,第二次过滤是为了得到固体
D.在pH>4的溶液中Fe3+一定不能大量存在.
19.下列对能量转化的认知中,不正确的是( )
| A. | 白炽灯工作时,电能全部转化为光能 | |
| B. | 风力发电时,风能主要转化为电能 | |
| C. | 煤燃烧时,化学能主要转化热能 | |
| D. | 电解水生成H2和O2时,电能主要转化为化学能 |
6.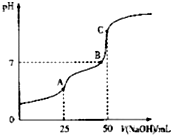 25°C时,向25ml 0.1wol•L-1 H2C2O4溶液中滴加同浓度的NaOH溶液,混合溶液的pH随滴加NaOH溶液体积的变化如图所示.下列有关叙述错误的是( )
25°C时,向25ml 0.1wol•L-1 H2C2O4溶液中滴加同浓度的NaOH溶液,混合溶液的pH随滴加NaOH溶液体积的变化如图所示.下列有关叙述错误的是( )
 25°C时,向25ml 0.1wol•L-1 H2C2O4溶液中滴加同浓度的NaOH溶液,混合溶液的pH随滴加NaOH溶液体积的变化如图所示.下列有关叙述错误的是( )
25°C时,向25ml 0.1wol•L-1 H2C2O4溶液中滴加同浓度的NaOH溶液,混合溶液的pH随滴加NaOH溶液体积的变化如图所示.下列有关叙述错误的是( )| A. | HC2O4-的电离程度大于其水解程度 | |
| B. | B点时溶液中含有NaHC2O4和Na2C2O4 | |
| C. | A点时,c(Na+)+c(H+)=c(OH-)+c(HC2O4-)+2c(C2O42-) | |
| D. | C点时,c(Na+)>c(C2O42-)>c(HC2O4-)>c(OH-)>c(H+) |
16.某原子的电子排布式为1s22s22p63s23p63d54s2,下列说法中不正确的是( )
| A. | 该元素原子中共有25个电子 | B. | 该元素原子核外有4个能层 | ||
| C. | 该元素原子最外层共有2个电子 | D. | 该元素原子M电子层共有8个电子 |
3.下列物质与其用途完全符合的是( )
①Na2O2-供氧剂
②晶体Si-太阳能电池
③AgI-人工降雨
④NaCl-制纯碱
⑤Al2O3-焊接钢轨
⑥NaClO-消毒剂
⑦Fe2O3-红色油漆或涂料
⑧SO2-食品防腐剂
⑨NH3-制冷剂
⑩水玻璃-耐火材料.
①Na2O2-供氧剂
②晶体Si-太阳能电池
③AgI-人工降雨
④NaCl-制纯碱
⑤Al2O3-焊接钢轨
⑥NaClO-消毒剂
⑦Fe2O3-红色油漆或涂料
⑧SO2-食品防腐剂
⑨NH3-制冷剂
⑩水玻璃-耐火材料.
| A. | ①④⑤⑧⑨ | B. | ①②③⑥⑦⑨ | C. | ①②③④⑥⑦⑨⑩ | D. | ①②③④⑥⑦⑨ |
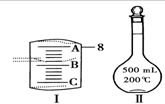 实验室要用Na2CO3•10H2O晶体配制500mLO.1mol•L-1Na2CO3溶液,回答下列问题:
实验室要用Na2CO3•10H2O晶体配制500mLO.1mol•L-1Na2CO3溶液,回答下列问题: