题目内容
19.在有机物A的分子中,同一个碳原子上连有3个甲基,5.1gA在空气中完全燃烧可生成0.3molCO2和6.3g水,等质量的A在127℃,1.01×105Pa时所占的体积为1.64L.A在铜催化剂的条件下与氧反应生成B,B能发生银镜反应.(1)求A的分子式;
(2)写出符合题意的A和B的结构简式和名称.
分析 (1)根据pV=nRT可知在压强、物质的量相同时,气体的体积与温度呈正比,据此可计算出标准状况下A的体积,再根据n=$\frac{V}{{V}_{m}}$计算出5.1gA的物质的量,从而可知A的摩尔质量;然后利用质量守恒定律确定A的分子式;
(2)根据A的分子式、结构及A、B具有的性质判断A、B的结构简式,然后根据有机物命名原则写出A、B的名称.
解答 解:(1)根据pV=nRT可知,在压强、物质的量相同时,气体的体积与温度呈正比,则等质量的A在127℃,1.01×105Pa时所占的体积为1.64L,在标准状况下体积为:1.64L×$\frac{273K}{(273+127)K}$=1.1193L,则5.1gA的物质的量为:$\frac{1.1193L}{22.4L/mol}$=0.05mol,A的摩尔质量为:$\frac{5.1g}{0.05mol}$=102g/mol,
6.3g水的物质的量为:$\frac{6.3g}{18g/mol}$=0.35mol,含有0.7molH原子,则A分子中含有C、H原子数为:N(C)=$\frac{0.3mol}{0.05mol}$=6、N(H)=$\frac{0.7mol}{0.05mol}$=14,A中含有C、H的总原子量为:12×6+1×14=86<102,则A分子中含有O元素,含有O的数目为:$\frac{102-86}{16}$=1,
所以A的分子式为:C6H14O,
答:A的分子式为C6H14O;
(2)A的分子式为C6H14O,在有机物A的分子中,同一个碳原子上连有3个甲基,A在铜催化剂的条件下与氧反应生成B,B能发生银镜反应,说明B分子中含有醛基,则A分子中含有羟基,其羟基位于末端C上,则A的结构简式为CH3C(CH3)2CH2CH2OH,名称为3,3-二甲基-1-丁醇;
A经过催化氧化生成醛B,则B的结构简式为(CH3)3CCH2CHO,名称为3,3-二甲基丁醛,
答:符合题意的A和B的结构简式和名称分别为:A.CH3C(CH3)2CH2CH2OH、3,3-二甲基-1-丁醇;B.(CH3)3CCH2CHO、3,3-二甲基丁醛.
点评 本题考查了有机物分子式、结构简式的确定,题目难度中等,明确常见有机物结构与性质为解答关键,注意掌握质量守恒定律在确定有机物分子式中的应用方法,试题培养了学生的分析能力及灵活应用能力.

| A. | Cl2+2KBr═Br2+2Cl2 | B. | 2Na2O2+2CO2═2Na2CO3+O2 | ||
| C. | 4Fe(OH)2+O2+2H2O═4Fe(OH)3 | D. | 2NaHCO3 $\frac{\underline{\;\;△\;\;}}{\;}$ Na2CO3+H2O+CO2↑ |
| A. | Al2O3难溶于水,不跟水反应,所以它不是Al(OH)3对应的氧化物 | |
| B. | 因为Al2O3是金属氧化物,所以它是碱性氧化物 | |
| C. | Al2O3属于两性氧化物 | |
| D. | Al2O3能与所有的酸、碱溶液反应 |
①Na2O2和CO2 ②NaOH和CO2 ③Na和O2 ④Na2CO3和HCl ⑤AlCl3和NaOH ⑥NaAlO2和CO2 ⑦Fe和HCl ⑧Ca(OH)2和NaHCO3.
| A. | ①⑥⑦⑧ | B. | ①⑥ | C. | ①⑦ | D. | ①④⑦ |
| A. | 化学家不可以制造出自然界不存在的材料 | |
| B. | 氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂 | |
| C. | Na2O2与水反应只能生成碱 | |
| D. | 高性能通信材料光导纤维的主要原料是硅 |
| A. |  除去CO中的CO2 | B. | 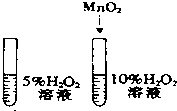 探究二氧化锰对反应速率的影响 | ||
| C. | 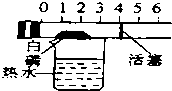 探究空气中氧气的含量 | D. |  探究溶解性的影响因素 |