题目内容
9.氧化还原反应与四种基本类型反应的关系如图所示,则下列化学反应属于阴影部分的是( )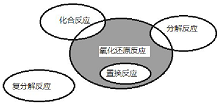
| A. | Cl2+2KBr═Br2+2Cl2 | B. | 2Na2O2+2CO2═2Na2CO3+O2 | ||
| C. | 4Fe(OH)2+O2+2H2O═4Fe(OH)3 | D. | 2NaHCO3 $\frac{\underline{\;\;△\;\;}}{\;}$ Na2CO3+H2O+CO2↑ |
分析 根据图象知阴影部分为不属于置换反应以及化合反应和分解反应的氧化还原反应,据此判断.
解答 解:A.Cl2+2KBr═Br2+2Cl2,属于一种单质与一种化合物生成另外一种单质与化合物的置换反应,不属于阴影部分,故A错误;B.过氧化钠与二氧化碳的反应不属于分解、化合和置换反应美术与阴影部分,故B正确;C.4Fe(OH)2+O2+2H2O═4Fe(OH)3属于化合反应,不属于阴影部分,故C错误;D.此反应没有元素化合价的变化不属于氧化还原反应,故D错误,故选B.
点评 本题考查了化学反应的四种基本反应类型和氧化还原反应的关系,难度不大,注意相关基础知识的积累.

练习册系列答案
相关题目
17.下列叙述正确的是( )
| A. | 浓盐酸具有强化性能将铜等不活泼金属氧化 | |
| B. | 稀硝酸与活泼金属反应主要放出氢气,而浓硝酸则使金属钝化 | |
| C. | 浓硝酸、稀硝酸和浓硫酸都是强氧化剂 | |
| D. | 在室温下,铜既可与浓硝酸反应,也可与浓硫酸反应 |
4.下列说法正确的是( )
| A. | 1mol H2O2中含有18NA个电子 | |
| B. | 阿伏加德罗常数的符号为NA,NA≈6.02×1023 | |
| C. | 阿伏加德罗常数是0.012kg C中所含的碳原子数 | |
| D. | 1mol OH-的质量为17g/mol |
14.下列说法不正确的是( )
| A. | 将wg质量分数为 a%的NaCl溶液加入wg水,得到的NaCl溶液质量分数一定为a/2% | |
| B. | 将wg质量分数为 a%的NaCl溶液蒸发掉w/2g水,得到的NaCl溶液质量分数一定为2a% | |
| C. | 现有10%和30%的氨水等质量混合后,溶液里溶质的质量分数为20% | |
| D. | 室温下向100ml1.2mol/l饱和石灰水中加入1.5g生石灰后恢复室温,石灰水中Ca(OH)2的物质的量不变 |
1. 重庆市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5μm的悬浮颗粒物),其主要来源为燃煤、机动车尾气等.因此,对PM2.5、SO2、NOx等进行研究具有重要意义.请回答下列问题:
重庆市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5μm的悬浮颗粒物),其主要来源为燃煤、机动车尾气等.因此,对PM2.5、SO2、NOx等进行研究具有重要意义.请回答下列问题:
(1)将PM2.5样本用蒸馏水处理制成待测试样.若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
根据表中数据判断PM2.5待测试样的pH约为4.
(2)为减少SO2的排放,常采取的措施有:将煤转化为清洁气体燃料.
已知:①2H2(g)+O2(g)═2H2O(g)K1 ②2C(s)+O2(g)═2CO(g)K2
C(s)+H2O(g)=CO(g)+H2(g) K=$(\frac{{K}_{1}}{{K}_{2}})^{\frac{1}{2}}$(用含K1、K2的式子表示).
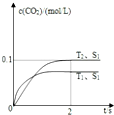
(3)汽车尾气净化的主要原理为:2NO(g)+2CO(g)?2CO2(g)+N2(g).在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线如图所示.
①在T2温度下,0~2s内的平均反应速率υ(N2)=0.025mol/(L•s).
②当固体催化剂的质量一定时,增大其表面积可提高化学反应速率.若催化剂的表面积S1>S2,在如图中画出c(CO2)在T1、S2条件下达到平衡过程中的变化曲线.
(4)①已知气缸中生成NO的反应为:N2(g)+O2(g)?2NO(g)△H>0,若1mol空气含0.8molN2和0.2molO2,1300℃时在密闭容器内反应达到平衡,测得NO为8×10-4mol.计算该温度下的平衡常数K=4×10-6.
②汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:2CO(g)═2C(s)+O2(g)已知该反应的△H>0,简述该设想能否实现的依据:不能实现,因为该反应是焓增、熵减的反应,△G=△H-T•△S>0.
 重庆市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5μm的悬浮颗粒物),其主要来源为燃煤、机动车尾气等.因此,对PM2.5、SO2、NOx等进行研究具有重要意义.请回答下列问题:
重庆市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5μm的悬浮颗粒物),其主要来源为燃煤、机动车尾气等.因此,对PM2.5、SO2、NOx等进行研究具有重要意义.请回答下列问题:(1)将PM2.5样本用蒸馏水处理制成待测试样.若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
| 离子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/mol•L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
(2)为减少SO2的排放,常采取的措施有:将煤转化为清洁气体燃料.
已知:①2H2(g)+O2(g)═2H2O(g)K1 ②2C(s)+O2(g)═2CO(g)K2
C(s)+H2O(g)=CO(g)+H2(g) K=$(\frac{{K}_{1}}{{K}_{2}})^{\frac{1}{2}}$(用含K1、K2的式子表示).
(3)汽车尾气净化的主要原理为:2NO(g)+2CO(g)?2CO2(g)+N2(g).在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线如图所示.
①在T2温度下,0~2s内的平均反应速率υ(N2)=0.025mol/(L•s).
②当固体催化剂的质量一定时,增大其表面积可提高化学反应速率.若催化剂的表面积S1>S2,在如图中画出c(CO2)在T1、S2条件下达到平衡过程中的变化曲线.
(4)①已知气缸中生成NO的反应为:N2(g)+O2(g)?2NO(g)△H>0,若1mol空气含0.8molN2和0.2molO2,1300℃时在密闭容器内反应达到平衡,测得NO为8×10-4mol.计算该温度下的平衡常数K=4×10-6.
②汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:2CO(g)═2C(s)+O2(g)已知该反应的△H>0,简述该设想能否实现的依据:不能实现,因为该反应是焓增、熵减的反应,△G=△H-T•△S>0.
18.下列图示的实验操作中,错误的是( )
| A. |  吸取液体 | B. |  称取一定质量的NaOH | ||
| C. |  铁在氧气中燃烧 | D. |  检查装置气密性 |
 ⑤ B.④⑤⑥ C.②③④ D.②④⑥
⑤ B.④⑤⑥ C.②③④ D.②④⑥