题目内容
盐酸、醋酸和碳酸氢钠是生活中常见的物质.下列表述正确的是( )
| A、在NaHCO3溶液中加入与其等物质的量的NaOH,溶液中的阴离子只有CO32-和OH- |
| B、NaHCO3溶液中:c(H+)+c(H2CO3)=c(OH-) |
| C、10mL 0.20mol?L-1 CH3COOH溶液加入10mL 0.10mol?L-1的NaOH后,溶液中:c(CH3COO-)+c(CH3COOH)=0.10mol?L-1 |
| D、中和体积与pH都相同的HCl溶液和CH3COOH溶液所消耗的NaOH物质的量相同 |
考点:离子浓度大小的比较,弱电解质在水溶液中的电离平衡,盐类水解的应用
专题:电离平衡与溶液的pH专题,盐类的水解专题
分析:A.碳酸钠是强碱弱酸盐能水解;
B.据物料守恒和电荷守恒判断;
C.醋酸钠是强碱弱酸盐,能发生水解,根据电荷守恒和物料守恒判断各种离子浓度之间的关系;
D.醋酸是弱酸,氢离子浓度小于醋酸浓度,根据醋酸和盐酸的物质的量确定消耗氢氧化钠的量.
B.据物料守恒和电荷守恒判断;
C.醋酸钠是强碱弱酸盐,能发生水解,根据电荷守恒和物料守恒判断各种离子浓度之间的关系;
D.醋酸是弱酸,氢离子浓度小于醋酸浓度,根据醋酸和盐酸的物质的量确定消耗氢氧化钠的量.
解答:
解:A.在NaHCO3溶液中加入与其等物质的量的NaOH,碳酸氢钠和氢氧化钠恰好反应生成碳酸钠,碳酸钠是强碱弱酸盐能水解,碳酸根离子水解生成碳酸氢根离子,碳酸氢根离子水解生成碳酸,导致溶液中阴离子含有CO32-、OH-、HCO3-,故A错误;
B.碳酸氢钠溶液中根据物料守恒知,C(Na+)=c (H2CO3)+c(HCO3-)+c(CO32-),根据电荷守恒知C(Na+)+c(H+)=c(OH-)+c(HCO3-)+2 c(CO32-),所以c(H+)+c(H2CO3)=c(OH-)+c(CO32-),故B错误;
C.10mL 0.20mol?L-1 CH3COOH溶液加入10mL 0.10mol?L-1的NaOH后,溶液体积增大为原来的2倍,则由物料守恒可知c(CH3COO-)+c(CH3COOH)=0.10mol?L-1,故C正确;
D.氯化氢是强电解质,醋酸是弱电解质,pH值相同的盐酸和醋酸,醋酸的浓度远远大于盐酸,所以等体积的盐酸和醋酸,醋酸的物质的量远远大于盐酸的物质的量,中和体积与pH都相同的HCl溶液和CH3COOH溶液,所消耗的NaOH醋酸的多,盐酸的少,故D错误.
故选C.
B.碳酸氢钠溶液中根据物料守恒知,C(Na+)=c (H2CO3)+c(HCO3-)+c(CO32-),根据电荷守恒知C(Na+)+c(H+)=c(OH-)+c(HCO3-)+2 c(CO32-),所以c(H+)+c(H2CO3)=c(OH-)+c(CO32-),故B错误;
C.10mL 0.20mol?L-1 CH3COOH溶液加入10mL 0.10mol?L-1的NaOH后,溶液体积增大为原来的2倍,则由物料守恒可知c(CH3COO-)+c(CH3COOH)=0.10mol?L-1,故C正确;
D.氯化氢是强电解质,醋酸是弱电解质,pH值相同的盐酸和醋酸,醋酸的浓度远远大于盐酸,所以等体积的盐酸和醋酸,醋酸的物质的量远远大于盐酸的物质的量,中和体积与pH都相同的HCl溶液和CH3COOH溶液,所消耗的NaOH醋酸的多,盐酸的少,故D错误.
故选C.
点评:本题考查了离子浓度大小的比较,为高考常见题型,侧重于学生的分析能力的考查,难度较大,能运用物料守恒和电荷守恒是解本题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
已知可以与盐酸反应的某溶液,分别与10mL浓度为2mol?L-1 的盐酸混合,并都加水稀释至50mL,其中反应速率最大的是( )
| A、10 mL 2 mol?L-1 |
| B、20 mL 2 mol?L-1 |
| C、10 mL 4 mol?L-1 |
| D、20 mL 3 mol?L-1 |
要使在容积恒定的密闭容器中进行的可逆反应2A(g)+B(s)?2C(g)的反应速率显著加快,可采用的措施是( )
| A、降温 | B、加入B |
| C、充入氦气,使压强增大 | D、加入A |
已知:HCN(aq)+NaOH(aq)═NaCN(aq)+H2O(l)△H=-12.1kJ?mol-1;
HCl(aq)+NaOH(aq)═NaCl(aq)+H2O(l)△H=-55.6kJ?mol-1
则HCN在水溶液中电离的△H等于( )
HCl(aq)+NaOH(aq)═NaCl(aq)+H2O(l)△H=-55.6kJ?mol-1
则HCN在水溶液中电离的△H等于( )
| A、+43.5 kJ?mol-1 |
| B、+67.7 kJ?mol-1 |
| C、-43.5 kJ?mol-1 |
| D、-67.7 kJ?mol-1 |
足量铜与一定量浓硝酸反应得到Cu(NO3)2溶液和NO2、NO的混合气体,这些气体与1.68L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸.若向所得Cu(NO3)2溶液中加入5mol?L-1 NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是( )
| A、60 mL |
| B、45 mL |
| C、30 mL |
| D、15 mL |
下列图示与对应的叙述相符的是( )
A、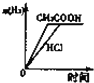 如图曲线表示向等体积、等物质的量浓度的盐酸和醋酸溶液中分别加人足量镁粉产生H2的物质的量的变化 |
B、 表示将0.01mol?L-1 NaOH溶液滴人到稀盐酸中的滴定曲线 |
C、 为水的电离曲线,从z点刭x点,可采用在水中加入适量NaOH固体的方法 |
D、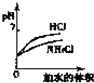 图中曲线表示将pH相同的NH4Cl溶液和盐酸稀释相同倍数时,二者pH的变化 |
下列说法不正确的是( )
| A、化学变化一定伴随着能量变化,伴随能量变化的过程未必是化学变化 |
| B、凡是有化学键断裂或形成的变化不一定是化学反应 |
| C、在光照下CH4与Cl2反应时,每一个Cl2分子可取代2个H原子 |
| D、放热反应必定是反应物的总能量>生成物的总能量 |
下列各组离子能在溶液中大量共存的是( )
| A、K+、Ag+、NO3-、S2- |
| B、Na+、Al3+、SO42-、HCO3- |
| C、NH4+、K+、OH-、SO42- |
| D、H+、Fe3+、Cl-、NO3- |