题目内容
草酸晶体的组成可表示为H2C2O4?xH2O,为测定x值,进行下列实验.
①称取m g草酸晶体,配成100.0mL溶液.
②取25.0mL所配草酸溶液置于锥形瓶中,加入适量稀H2SO4后,用浓度为c mol?L-1 KMnO4溶液滴定.滴定时,所发生反应为:2KMnO4+5H2C2O4+3H2SO4═K2SO4+10CO2↑+2MnSO4+8H2O.请回答下列问题:
(1)实验①中为了配制准确浓度的草酸溶液,所需要的实验仪器主要有:天平(含砝码)、烧杯、药匙、玻璃棒、胶头滴管和 .
(2)在实验②中,滴定时KMnO4溶液应装在 (填“酸式”或“碱式”)滴定管中,锥形瓶中 (填“需要”或“不需要”)滴加指示剂.
(3)在滴定过程中,目光应注视 .
(4)若滴定时,滴定前后两次读数分别为a mL和b mL,因此计算出草酸晶体x值为 .
①称取m g草酸晶体,配成100.0mL溶液.
②取25.0mL所配草酸溶液置于锥形瓶中,加入适量稀H2SO4后,用浓度为c mol?L-1 KMnO4溶液滴定.滴定时,所发生反应为:2KMnO4+5H2C2O4+3H2SO4═K2SO4+10CO2↑+2MnSO4+8H2O.请回答下列问题:
(1)实验①中为了配制准确浓度的草酸溶液,所需要的实验仪器主要有:天平(含砝码)、烧杯、药匙、玻璃棒、胶头滴管和
(2)在实验②中,滴定时KMnO4溶液应装在
(3)在滴定过程中,目光应注视
(4)若滴定时,滴定前后两次读数分别为a mL和b mL,因此计算出草酸晶体x值为
考点:中和滴定,化学史
专题:实验设计题
分析:(1)实验①中为了配制准确浓度的草酸溶液,所需要的实验仪器主要有天平(含砝码)、烧杯、药匙、100mL容量瓶、胶头滴管、玻璃棒等;
(2)KMnO4溶液具有强氧化性,可以腐蚀橡皮管,故KMnO4溶液应装在酸式滴定管中;
KMnO4溶液呈紫色,草酸反应完毕,滴入最后一滴KMnO4溶液,紫色不褪去,说明滴定到终点,不需要外加指示剂;
(3)在滴定过程中,目光应注视锥形瓶中溶液颜色的变化;
(4)滴定管的刻度由上而下刻度增大,滴定前后两次读数分别为amL和bmL,故消耗KMnO4溶液体积(b-a)mL,根据关系式2KMnO4~5H2C2O4计算25.0mL草酸溶液中n(H2C2O4),进而计算100mL草酸溶液中n′(H2C2O4),计算草酸的质量,根据化学式质量分数的计算求X的值.
(2)KMnO4溶液具有强氧化性,可以腐蚀橡皮管,故KMnO4溶液应装在酸式滴定管中;
KMnO4溶液呈紫色,草酸反应完毕,滴入最后一滴KMnO4溶液,紫色不褪去,说明滴定到终点,不需要外加指示剂;
(3)在滴定过程中,目光应注视锥形瓶中溶液颜色的变化;
(4)滴定管的刻度由上而下刻度增大,滴定前后两次读数分别为amL和bmL,故消耗KMnO4溶液体积(b-a)mL,根据关系式2KMnO4~5H2C2O4计算25.0mL草酸溶液中n(H2C2O4),进而计算100mL草酸溶液中n′(H2C2O4),计算草酸的质量,根据化学式质量分数的计算求X的值.
解答:
解:(1)实验①中为了配制准确浓度的草酸溶液,所需要的实验仪器主要有天平(含砝码)、烧杯、药匙、100mL容量瓶、胶头滴管、玻璃棒等,故还需要100mL容量瓶、胶头滴管、玻璃棒,故答案为:100mL容量瓶;
(2)KMnO4溶液具有强氧化性,可以腐蚀橡皮管,故KMnO4溶液应装在酸式滴定管中;
KMnO4溶液呈紫色,草酸反应完毕,滴入最后一滴KMnO4溶液,紫色不褪去,说明滴定到终点,不需要外加指示剂,
故答案为:酸式;不需要;
(3)在滴定过程中,目光应注视锥形瓶中溶液颜色的变化,故答案为:锥形瓶中溶液颜色的变化;
(4)滴定管的刻度由上而下刻度增大,滴定前后两次读数分别为amL和bmL,故消耗KMnO4溶液体积(b-a)mL,n(KMnO4)
=c mol?L-1×(b-a)×10-3L=c×(b-a)×10-3mol,根据关系式2KMnO4~5H2C2O4可知25.0mL草酸溶液中n(H2C2O4)=2.5×c×(b-a)×10-2mol,进而计算100mL草酸溶液中n′(H2C2O4)=2.5×c×(b-a)×10-2mol×
=c×(b-a)×10-2mol,草酸晶体中草酸的质量为c×(b-a)×10-2mol×90g/mol=0.9c(b-a)g,由化学式可知:
=
,解得x=
-5,故答案为:
-5.
(2)KMnO4溶液具有强氧化性,可以腐蚀橡皮管,故KMnO4溶液应装在酸式滴定管中;
KMnO4溶液呈紫色,草酸反应完毕,滴入最后一滴KMnO4溶液,紫色不褪去,说明滴定到终点,不需要外加指示剂,
故答案为:酸式;不需要;
(3)在滴定过程中,目光应注视锥形瓶中溶液颜色的变化,故答案为:锥形瓶中溶液颜色的变化;
(4)滴定管的刻度由上而下刻度增大,滴定前后两次读数分别为amL和bmL,故消耗KMnO4溶液体积(b-a)mL,n(KMnO4)
=c mol?L-1×(b-a)×10-3L=c×(b-a)×10-3mol,根据关系式2KMnO4~5H2C2O4可知25.0mL草酸溶液中n(H2C2O4)=2.5×c×(b-a)×10-2mol,进而计算100mL草酸溶液中n′(H2C2O4)=2.5×c×(b-a)×10-2mol×
| 100mL |
| 25mL |
| 90 |
| 90+18x |
| 0.9c(b-a)g |
| mg |
| 50m |
| 9c?(b-a) |
| 50m |
| 9c?(b-a) |
点评:本题考查一定物质的量浓度溶液配制、滴定操作、滴定应用与计算、物质组成含量测定等,难度中等,注意滴定中经常根据关系式进行计算,掌握根据关系式计算方法.

练习册系列答案
 天天向上口算本系列答案
天天向上口算本系列答案
相关题目
将8.4克铁粉和3.2克硫粉混和隔绝空气加热,使之充分反应,再将反应后的物质与足量的稀H2SO4反应,可得到气体体积(标况下)是( )
| A、1.12L | B、2.24L |
| C、3.36L | D、都不对 |
下列有关物质分类或归类错误的是( )
| A、混合物:盐酸、生铁、空气 |
| B、化合物:CaCl2、NaOH、HCl |
| C、碱:苛性钠、纯碱、氢氧化钾 |
| D、单质:Ca、O3、石墨 |
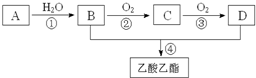 已知:A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平.现以A为主要原料合成乙酸乙酯,其合成路线如图所示.
已知:A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平.现以A为主要原料合成乙酸乙酯,其合成路线如图所示.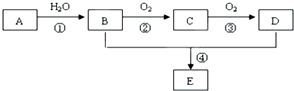
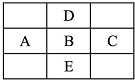 如图是周期表的一部分,A、B、C、D、E五种元素的原子核共含有80个质子.
如图是周期表的一部分,A、B、C、D、E五种元素的原子核共含有80个质子. 原子序数由小到大排列的四种短周期元素X、Y、Z、W,四种元素的原子序数之和为32,在周期表中X是原子半径最小的元素,Y、Z左右相邻,Z、W位于同主族.
原子序数由小到大排列的四种短周期元素X、Y、Z、W,四种元素的原子序数之和为32,在周期表中X是原子半径最小的元素,Y、Z左右相邻,Z、W位于同主族.