题目内容
将8.4克铁粉和3.2克硫粉混和隔绝空气加热,使之充分反应,再将反应后的物质与足量的稀H2SO4反应,可得到气体体积(标况下)是( )
| A、1.12L | B、2.24L |
| C、3.36L | D、都不对 |
考点:化学方程式的有关计算
专题:计算题
分析:加热发生反应Fe+S
FeS,加入稀H2SO4一定发生反应FeS+H2SO4=FeSO4+H2S↑,而Fe与硫酸反应为Fe+H2SO4=FeSO4+H2↑,由方程式可知加热过程中Fe无论过量与否,与硫酸反应最终得到的气体的物质的量等于原混合物中Fe的物质的量,再根据V=nVm计算生成气体的体积.
| ||
解答:
解:热发生反应Fe+S
FeS,加入稀H2SO4一定发生反应FeS+H2SO4=FeSO4+H2S↑,而Fe与硫酸反应为Fe+H2SO4=FeSO4+H2↑,由方程式可知加热过程中Fe无论过量与否,与硫酸反应最终得到的气体的物质的量等于原混合物中Fe的物质的量,故n(气体)=n(Fe)=
=0.15mol,气体体积为0.15mol×22.4L/mol=3.36L,
故选C.
| ||
| 8.4g |
| 56g/mol |
故选C.
点评:本题考查混合物计算、根据方程式的计算,难度中等,充分利用方程式判断生成气体与原混合物中Fe的物质的量相等,避免加热过程中的过量计算的繁琐,侧重对学生综合能力的考查.

练习册系列答案
相关题目
元素周期表中ⅣA元素包括C、Si、Ce、Sn、Pb等,已知Sn的+4价稳定,而Pb的+2价稳定.结合所学知识,判断下列反应中(反应条件略)正确的是( )
①Pb+2Cl2=PbCl4
②Sn+2Cl2=SnCl4
③SnCl2+Cl2=SnCl4
④PbO2+4HCl=PbCl4+2H2O
⑤Pb3O4+8HCl=3PbCl2+Cl2↑+4H2O.
①Pb+2Cl2=PbCl4
②Sn+2Cl2=SnCl4
③SnCl2+Cl2=SnCl4
④PbO2+4HCl=PbCl4+2H2O
⑤Pb3O4+8HCl=3PbCl2+Cl2↑+4H2O.
| A、①②④⑤ | B、①②③④ |
| C、①②③ | D、②③⑤ |
下列有关说法不正确的是( )
| A、C3H8中碳原子都采用的是sp3杂化 |
| B、O2、CO2、N2都是非极性分子 |
| C、酸性:H2CO3<H3PO4<H2SO4<HClO |
D、CO的一种等电子体为NO+,它的电子式为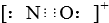 |
已知M2O7x-+3S 2-+14H+=2M3++3S↓+7H2O,则M2O7x-中的M的化合价为( )
| A、+2价 | B、+3价 |
| C、+4价 | D、+6价 |
已知:一般溶液浓度越大密度越大,氨水等例外.则体积为vL、质量为mg,浓度为a mol/L的氨水溶液的溶质质量分数为b%,用水稀释到0.5a mol/L,下列说法正确的是( )
| A、加水的体积为vL |
| B、加水的质量为mg |
| C、0.5amol/L的氨水质量分数等于0.5b% |
| D、0.5amol/L的氨水质量分数小于0.5b% |
下列数量的物质中含原子数最多的是( )
| A、0.4 mol氧气 |
| B、标准状况下5.6 L二氧化碳 |
| C、4°C时5.4 mL水 |
| D、10 g氦气 |
在0.5L某浓度的Na2SO4溶液中含有0.5mol Na+,对该溶液的说法不正确的是( )
| A、该溶液的物质的量浓度为1 mol?L-1 |
| B、该溶液中含有35.5 g Na2SO4 |
| C、配制100 mL该溶液需用7.1 g Na2SO4 |
| D、量取100 mL该溶液倒入烧杯中,烧杯中Na+的物质的量为0.1 mol |